题目内容
【题目】四氢呋喃 (THF)常用于药物合成,结构如下图,下列关于该化合物的说法错误的是
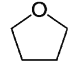
A.二氯代物有五种
B.与丁醛互为同分异构体
C.所有碳原子不能处于同一平面
D.1mol呋喃(![]() )生成1 mol 四氢呋喃需要2 mol H2
)生成1 mol 四氢呋喃需要2 mol H2
【答案】A
【解析】
A.由四氢呋喃的结构简式,一个碳原子上的两个氢原子被两个氯原子代替有两种结构 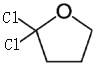 、
、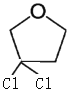 ,当两个氯原子不再同一个碳原子上时,
,当两个氯原子不再同一个碳原子上时,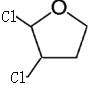 、
、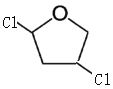 、
、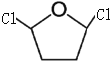 、
、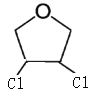 ,故四氢呋喃的二氯代物有6种,A错误;
,故四氢呋喃的二氯代物有6种,A错误;
B.四氢呋喃与丁醛的分子式都是C4H8O,但是结构不同,故它们互为同分异构体,B正确;
C.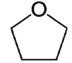 分子中所有的碳原子都是采用sp3杂化,故该分子中所有碳原子不能处于同一平面,C正确;
分子中所有的碳原子都是采用sp3杂化,故该分子中所有碳原子不能处于同一平面,C正确;
D.1个呋喃(![]() )分子中含有2个碳碳双键,故1mol呋喃(
)分子中含有2个碳碳双键,故1mol呋喃(![]() )生成1 mol 四氢呋喃需要2 mol H2,D正确;
)生成1 mol 四氢呋喃需要2 mol H2,D正确;
答案选A。

【题目】党的十九大报告中多次提及“绿色环保”、“生态文明”,而 CO2 的有效利用可以缓解温室效应,解决能源短缺问题。
(1)某研究所的科研人员在新型纳米催化剂 Na-Fe3O4 和 HMCM-22 的表面,以 CO2 为碳源,与电解水产生的 H2 催化转化为高附加值的烃类化合物,其过程如图。
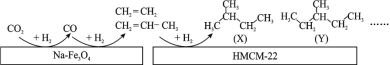
图中 CO2 转化为 CO 的反应为:CO2(g) + H2(g)=CO(g) + H2O(g) ΔH1 = + 41 kJmol-1。已知:2CO2(g) + 6H2(g)=C2H4(g) + 4H2O(g) ΔH2=-128 kJmol-1。图中 CO 转化为 C2H4 的热化学方程式是__________________ 。
(2)甲醇是未来重要的绿色能源之一,在工业中常用 CO、H2 合成甲醇,其反应为:CO(g)+2H2(g)CH3OH(g) ΔH3 < 0
①为了探究浓度对反应速率的影响,200℃ 时在 10 L 恒容密闭容器中进行实验,测得的实验数据如下表所示:
实验 | 起始浓度/(mol·L-1) | 初始速率/(mol·L-1·min-1) | |
CO | H2 | ||
1 | 0.25 | 0.50 | 0.391 |
2 | 0.25 | 1.00 | 0.781 |
3 | 0.50 | 0.50 | 0.780 |
该反应速率的通式为 v正=k正 cm(CO)cn(H2)(k 正是与温度有关的速率常数)。由表中数据可确定反应速率通式中 m =_______、n =_____(取正整数)。实验发现,当实验 1 中 c(H2) = 0.25 molL-1时达到平衡,请计算该反应的平衡常数 K = _____。
②若将一定比例的 CO 和 H2 在装有催化剂的反应器中反应 12 小时,体系中甲醇的产率和催化剂的催化活性与温度的关系如图所示。
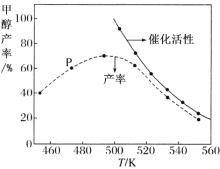
请判断温度为 470 K 时,图中 P 点 _________(填“是”或“不是”)处于平衡状态,490 K 之后,甲醇产率随温度升高而减小的可能原因为:_____、 _____。
(3)近年来,有研究人员用 CO2 通过电催化生成多种燃料,其工作原理如图所示。
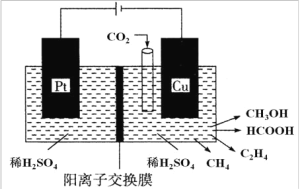
①请写出 Cu 电极上产生 CH3OH 的电极反应式:_____________。
②如果Cu 电极上只生成 0.15 mol C2H4 和 0.30 mol CH3OH,则 Pt 电极上产生O2 的物质的量为 ___________mol。
③已知 HCOOH 为一元弱酸,常温下将 0.1 molL-1 HCOOH 溶液与 0.1 molL-1 NaOH 溶液按体积比 a : b混和(忽略溶液体积的变化),混合后溶液恰好显中性,则 HCOOH 的电离常数 Ka=_____________(用含 a、b 的代数式表示)。