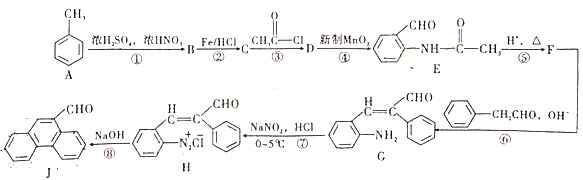
题目内容
【题目】某同学利用生活中或实验室中常用的物品,根据氧化还原反应知识和电化学知识,自己动手设计了一个原电池。请填写下列空白:
(1)实验原理:Fe+2H+=Fe2++H2↑
(2)实验用品:电极(______、______)、稀硫酸、______、________、耳机(或者电流表)(填写所缺的实验用品)。
(3)实验装置如图。
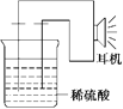
(4)原电池设计及注意的问题:
①按如图所示装置连接好实验仪器,注意观察(耳朵听)耳机是否有声音发出,如果没有,可将原电池的两个电极中的一极接触耳机插头上的一极(注意:接触的同时耳机的另一个极是连接在原电池的另一个电极上的),这时可以听见耳机发生“嚓嚓嚓……”的声音。其原因是在原电池中,由化学能转化为____________,在耳机中又由__________转化为声音这种能量;
②如果将装置中的耳机改为电流表,则铁钉应该接电流表的________极,电极反应式为_____________,发生了________反应;
③铜钉应该接电流表的________极,电极反应式为_____________,发生了_________反应。
【答案】铁钉或铁条 铜钉(其他的惰性电极如铅笔芯、铂等都正确) 烧杯 导线 电能 电能 负 Fe-2e-=Fe2+ 氧化 正 2H++2e-=H2↑ 还原
【解析】
由反应Fe+2H+=Fe2++H2↑可知,反应中Fe被氧化,应为原电池的负极,则正极可为活泼性较铁弱的金属或非金属单质,结合形成原电池的条件以及能量的转化形式分析解答。
(2)由形成原电池的条件结合反应原理Fe+2H+=Fe2++H2↑可知,需要铁为负极,正极为铜钉(其他的惰性电极如铅笔 芯、铂等都可以),硫酸为电解质溶液,还需要烧杯、导线等,故答案为:铁钉或铁条;铜钉(其他的惰性电极如铅笔 芯、铂等都可以);烧杯;导线;
(4)①在原电池中,化学能转化为电能,在耳机中又由电能转化为声音这种能量,故答案为:电能;电能;
②在原电池中,铁为负极,发生氧化反应,电极方程式为Fe-2e-=Fe2+,铜为正极,发生还原反应,电极方程式为2H++2e-=H2↑,如果将装置中的耳机改为电流计,铁钉应该接电流表的负极,电流表指针发生偏转,故答案为:负;Fe-2e-=Fe2+;氧化;
③根据②的分析,铜为正极,发生还原反应,电极方程式为2H++2e-=H2↑,应该接电流表的正极,故答案为:正;2H++2e-=H2↑;还原。