题目内容
元素X形成的离子与钙离子的核外电子排布相同,且X的离子半径小于负二价硫离子的半径.X元素为( )
A.Al B.P C.Ar D.K
D
【解析】电子层结构相同的微粒,核电荷数越大,半径越小.
【解析】
由题意可知,元素X形成的离子中,K、L、M电子层上的电子数分别为2、8、8,
与S2﹣的电子层结构相同,对于电子层结构相同的离子,核电荷数越大,半径越小,故X的核电荷数应大于S的核电荷数,符合要求的元素是K,
故选D.

 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案(12分)甲同学拟通过实验探究同主族元素性质的递变规律,以及影响化学反应速率的因素。其设计的实验方案如下,请你帮他填写完整,并做出评价。
实验室提供的试剂:锌块、锌粉、铁条、铁粉、铜条、NaBr溶液、NaI溶液、新制的氯水、1mol/L盐酸、3mol/L的盐酸
(1)探究同主族元素性质的递变规律
①写出下列实验报告中的实验现象和离子方程式
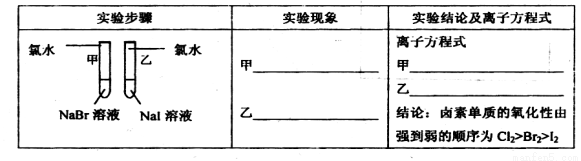
②【评价】甲同学设计的实验方案的合理性是___________(填序号)
A. 非常合理B. 部分合理C. 完全不合理
③【补充和完善】上一题②中若选A,则此项不用再作答,若选B或C,则完成实验还需要的试剂是___________。
(2)探究影响化学反应速率的因素
实验步骤 | 实验现象 | 实验依据和结论 |
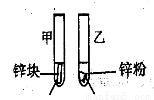
3mL1mol/L 3mL3mol/L 盐酸 盐酸 (金属质量相同,盐酸均过量) | 均有气体生成,锌粉先消失,锌块后消失 | 因为乙试管中的反应更快,所以反应物浓度越大,反应速率越快。 |
甲同学所得实验依据和结论有明显问题,问题是 。
(3)请你利用原电池原理,设计实验,比较铜和铁的金属活动性。画出实验装置图,标出正负极、电子流动方向,写出电极反应式。
现有部分元素的性质与原子(或分子)结构如下表:
元素编号 | 元素性质与原子(或分子)结构 |
T | 最外层电子数是次外层电子数的3倍 |
X | 常温下单质为双原子分子,分子中含有3对共用电子对 |
Y | M层比K层少1个电子 |
Z | 第3周期元素的简单离子中半径最小 |
(1)画出元素T的原子结构示意图__________________________;
(2)元素Y与元素Z相比,金属性较强的是__________________(用元素符号表示),下列表述中能证明这一事实的是_________________(填序号);
a.Y单质的熔点比Z单质低b.Y的化合价比Z低
c.Y单质与水反应比Z单质剧烈d.Y最高价氧化物的水化物的碱性比Z强
(3)T、X、Y、Z中有两种元素能形成既有离子键又有非极性共价键的化合物,写出该化合物的化学式___________,并写出该化合物与水反应的离子方程式______;
(4)元素T和氢元素以原子个数比1∶1化合形成的化合物属于______________,元素Z与元素T形成的化合物属于____________________(以上两空选填“共价化合物”或“离子化合物”)。