题目内容
【题目】现有铁、碳两种元素组成的合金,某实验小组为了研究该合金的性质并测定该合金中碳的质量分数,设计了如下实验方案和实验装置:

(1)取ag合金粉末放入蒸馏烧瓶,并加入足量浓硫酸,A、B中均无明显现象,原因是________________________________________________。
(2)反应一段时间后,B中的现象为___________________________。
(3)装置C的作用是________________;装置D的作用是___________,F的作用是___________________________________________。
(4)反应结束后,若U形管E增重m g,则合金中碳的质量分数为________。(用含m和a的式子表示)
【答案】常温下Fe在浓硫酸中钝化,碳不与浓硫酸反应 品红溶液红色褪去 除去二氧化硫 除去水蒸气 防止空气中的水蒸气和CO2进入E,减少实验误差 ![]() ×100%
×100%
【解析】
铁和碳单质均可以和浓硫酸反应生成二氧化碳、二氧化硫,二氧化硫的检验可以用品红,吸收可以用高猛酸钾,将产生的二氧化碳用浓硫酸干燥,通入碱石灰,根据碱石灰增加的质量可以确定二氧化碳的质量,根据C元素守恒,可以计算碳单质的质量,进而计算碳的质量分数,据此解答。
(1) 往A中滴加足量的浓硫酸,未点燃酒精灯前,A、B均无明显现象,常温下铁在浓硫酸中钝化,碳和浓硫酸在加热条件下才能反应;
故答案为:常温下Fe在浓硫酸中钝化,碳不与浓硫酸反应;
(2)由于铁、碳与浓硫酸发生反应时均有二氧化硫生成,二氧化硫具有漂白性,在盛有品红溶液的B试管中,通入二氧化硫,溶液褪色;
故答案为:品红溶液红色褪去;
(3)该实验测定二氧化碳的质量,进而计算合金中碳的质量分数。因此装置C盛有高锰酸钾溶液,可以吸收二氧化硫气体,装置D中浓硫酸是吸收其他中的水蒸气,除去水蒸气;F中的碱石灰可防止空气中的水蒸气和CO2进入E。
故答案为:除去二氧化硫;除去水蒸气;防止空气中的水蒸气和CO2进入E,减少实验误差;
(4)U形管增加的质量即为二氧化碳的质量,根据碳元素守恒,合金中碳的质量为![]() ×12 g/mol=
×12 g/mol=![]() g,所以合金中碳的质量分数为
g,所以合金中碳的质量分数为![]() ×100%。
×100%。
故答案为:![]() ×100%。
×100%。

【题目】下列图中的实验方案,能达到实验目的的是
选项 | 实验方案 | 实验目的 |
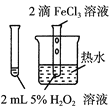
A |
| 验证FeCl3对H2O2分解反应有催化作用 |
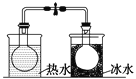
B |
将NO2球浸泡在冰水和热水中 | 探究温度对平衡2NO2 |
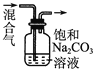
C |
| 除去CO2气体中混有的SO2 |
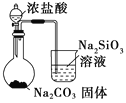
D |
| 比较HCl、H2CO3和H2SiO3的酸性强弱 |
A. A B. B C. C D. D
【题目】运用图示装置完成相关实验合理的是
选项 | ①中物质 | ②中物质 | 实验目的 | 装置 |
A | 乙醇 | K2Cr2O7溶液 | 验证乙醇的还原性 |
|
B | 浓盐酸 | KMnO4固体 | 制取并收集氯气 | |
C | 少量氯化铝溶液 | 浓氢氧化钠溶液 | 制取氢氧化铝沉淀 | |
D | 稀硝酸 | 铜粉 | 制取并收集NO |
A. A B. B C. C D. D