��Ŀ����
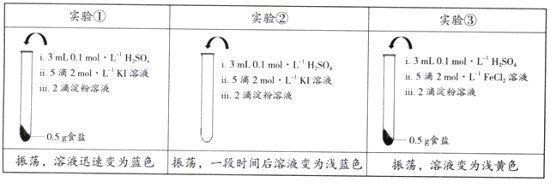
����Ŀ��Ϊ����ij�ӵ�ʳ�����Ƿ���KIO3��ȡ��ͬʳ����Ʒ�����±���ʾʵ�飺
����֪��KIO3 + 5KI + 3H2SO4![]() 3I2 + 3K2SO4 + 3H2O��
3I2 + 3K2SO4 + 3H2O��
����˵������ȷ����
A. ����ʵ��پ���֤��ʳ����Ʒ�д���KIO3
B. ʵ����з�����Ӧ�����ӷ���ʽΪ4I��+ O2 + 4H+ ![]() 2I2 + 2H2O
2I2 + 2H2O
C. ʵ�����֤��ʳ����Ʒ�в�����KIO3
D. ����ʵ��˵�����ӵĻ�ԭ�ԣ�I�� > Fe2+
���𰸡�B
��������A. ʵ����п����ǵ⻯�������������±������е���������������֤��ʳ���д���KIO3����A����B. ʵ��ڵ⻯�������������±������е�������������Ӧ�����ӷ���ʽΪ4I��+ O2 + 4H+ = 2I2 + 2H2O����B��ȷ��C. ʵ�����Һ��dz��ɫ��Ϊ�����ӵ���ɫ��˵���������ӱ������������DZ������е������������п����DZ������������˵��ʳ����Ʒ�п��ܴ���KIO3����C����D. ��������ʵ�飬����˵���������ܹ������������������˵���������ܹ�����������������˵�����������ܹ�����������������������ʵ�鲻���ж�I�� ��Fe2+���ӵĻ�ԭ�ԣ���D����ѡB��

��ϰ��ϵ�д�
�����Ŀ