题目内容
16.将40mL密度为1.84g•mL-1的98%浓硫酸缓缓加人200mL水中配成稀硫酸.测得稀硫酸的密度是1.2g•mL-1,则稀硫酸中溶质的质量分数是26.5%,物质的量浓度是3.2mol/L.分析 浓硫酸中m(H2SO4)=1.84g•mL-1×40mL×98%=72.128g,加入200mL水配制成稀硫酸溶液,稀硫酸溶液质量=72.128g+200g=272.128g,稀硫酸中溶质质量分数=$\frac{硫酸质量}{稀硫酸质量}×100%$;
稀硫酸体积=$\frac{272.128g}{1200g/L}$=0.227L,根据c=$\frac{n}{V}$计算稀硫酸物质的量浓度.
解答 解:浓硫酸中m(H2SO4)=1.84g•mL-1×40mL×98%=72.128g,加入200mL水配制成稀硫酸溶液,稀硫酸溶液质量=72.128g+200g=272.128g,稀硫酸中溶质质量分数=$\frac{硫酸质量}{稀硫酸质量}×100%$=$\frac{72.128g}{272.128g}×100%$=26.5%;
稀硫酸体积=$\frac{272.128g}{1200g/L}$=0.227L,稀硫酸c=$\frac{n}{V}$=$\frac{\frac{72.128g}{98g/mol}}{0.227L}$=3.2mol/L,
故答案为:26.5%;3.2mol/L.
点评 本题考查物质的量浓度、质量分数有关计算,侧重考查学生分析计算能力,明确公式中各个物理量的关系是解本题关键,知道稀硫酸体积计算方法,为易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.英国曼彻斯特大学科学家安德烈•海姆和康斯坦丁•诺沃肖洛夫以石墨烯研究获得2010年度诺贝尔物理学奖.石墨烯可看作将石墨的层状结构一层一层的剥开得到的单层碳原子构成的二维蜂窝状晶格结构(如图所示).石墨烯是现在已知的最牢固的一种碳质新材料,有极佳的导电、导热性.下列说法正确的是( )

| A. | 石墨烯是一种有机物 | B. | 石墨烯中碳原子间以共价键结合 | ||
| C. | 石墨烯具有和乙烯相同的性质 | D. | 12g石墨烯中约含6.02×1023个e- |
11.化学与社会生产、生活密切相关.下列做法错误的是( )
| A. | 太阳能电池板中的硅在元素周期表中处于金属与非金属的交界位置 | |
| B. | 提倡步行、骑自行车、乘公交车等“低碳”出行方式 | |
| C. | 明矾在自来水的生产过程中,常用于杀菌消毒 | |
| D. | 开发利用各种新能源,减少对化石燃料的依赖,可以降低空气中PM2.5的含量 |
8.反应4A(s)+3B(g)=2C(g)+D(g),经2min,B的浓度减少0.6mol•L-1,对此反应速率的表示正确的是 ( )
| A. | 用A表示的反应速率为0.4 mol•L-1•min-1 | |
| B. | 分别用A、B、C、D表示的反应速率其比值为4:3:2:1 | |
| C. | 在2 min末的反应速率,用B表示是0.3 mol•L-1•min-1 | |
| D. | 在这2 min内用B和C表示的反应速率都是逐渐减小的 |
5.在0.5mol Na2SO4中,含有的氧原子个数约为( )
| A. | 1.204×1024 | B. | 0.5 | C. | 6.02×1023 | D. | 3.01×1023 |

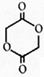 ;C中所含官能团的名称是羧基、溴原子.
;C中所含官能团的名称是羧基、溴原子.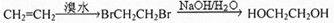 .
.