题目内容
【题目】用Cl2生产某些含氯有机物时会产生副产物HCl.利用反应A可实现氯的循环利用.反应A:4HCl+O2 ![]() 2Cl2+2H2O 已知:ⅰ.此条件下反应A中,4mol HCl被氧化,放出115.6kJ的热量.
2Cl2+2H2O 已知:ⅰ.此条件下反应A中,4mol HCl被氧化,放出115.6kJ的热量.
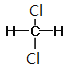
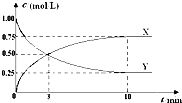
ⅱ. ![]()
①写出此条件下,反应A的热化学方程式 .
②断开1mol H﹣O键与断开1mol H﹣Cl键所需能量相差约为kJ.
【答案】4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)△H=﹣115.6 KJ/mol;31.9
【解析】解:①反应4HCl+O2 ![]() 2Cl2+2H2O中,4mol HCl被氧化,放出115.6kJ的热量,则反应的热化学方程式为:4HCl(g)+O2(g)2Cl2(g)+2H2O(g)△H=﹣115.6 kJ/mol,
2Cl2+2H2O中,4mol HCl被氧化,放出115.6kJ的热量,则反应的热化学方程式为:4HCl(g)+O2(g)2Cl2(g)+2H2O(g)△H=﹣115.6 kJ/mol,
所以答案是:4HCl(g)+O2(g)2Cl2(g)+2H2O(g)△H=﹣115.6 kJ/mol;
②焓变=反应物断键吸收热量﹣生成物形成化学键放出热量,4HCl(g)+O2(g)2Cl2(g)+2H2O(g)△H=﹣115.6 kJ/mol,
则该反应的焓变△H=4×E(H﹣Cl)+498﹣[243×2+4×E(H﹣O)]=﹣115.6,
即:4×E(H﹣O)﹣4×E(H﹣Cl)=498﹣486+115.6=127.6,整理可得:E(H﹣O)﹣E(H﹣Cl)=31.9,
所以答案是:31.9.
【考点精析】根据题目的已知条件,利用反应热和焓变的相关知识可以得到问题的答案,需要掌握在化学反应中放出或吸收的热量,通常叫反应热.

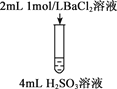
【题目】下列三组实验进行一段时间后,溶液中均有白色沉淀生成,下列结论不正确的是
实验① | 实验② | 实验③ |
|
|
|
A. 实验①中生成的沉淀是BaCO3
B. 实验①中有气体生成
C. 实验②沉淀中可能含有BaSO4
D. 实验③生成沉淀的离子方程式是:Ba2++ H2SO3===BaSO3↓+2H+