题目内容
16.NA为阿伏伽德罗常数的值,下列说法正确的是( )| A. | 25℃时,1LpH=l的HCl溶液中,由水电离的H+的个数为0.1NA | |
| B. | 25℃时,0.1mol/LNaHCO3溶液中含有HCO3-数小于0.1NA | |
| C. | 标准状况下,NA个H2O分子所占有的体积约为22.4L | |
| D. | lmol(NH4)2Fe(SO4)2•6H2O固体中含有离子总数为5NA |
分析 A、在HCl溶液中水的电离被抑制;
B、溶液体积不明确;
C、标况下,水为液体;
D、(NH4)2Fe(SO4)2•6H2O由2个铵根离子、1个亚铁离子和2个硫酸根离子以及6个水分子构成.
解答 解:A、在HCl溶液中水的电离被抑制,氢离子绝大多数来自HCl的电离,氢氧根全部来自水的电离,而pH=1的盐酸溶液中,氢氧根浓度为10-13mol/L,故1L溶液中氢氧根的物质的量为10-13mol,而水电离出的氢离子的物质的量和氢氧根的物质的量相同,故此溶液中水电离出的氢离子的个数为10-13NA个,故A错误;
B、溶液体积不明确,故此溶液中的碳酸氢根的个数无法计算,故B错误;
C、标况下,水为液体,故NA个水分子即1mol水的体积小于22.4L,故C错误;
D、(NH4)2Fe(SO4)2•6H2O由2个铵根离子、1个亚铁离子和2个硫酸根离子以及6个水分子构成,故1mol(NH4)2Fe(SO4)2•6H2O固体中含5mol离子即5NA个离子,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
7.下列叙述中,错误的是( )
| A. | 炼铁时,还原剂CO将铁从铁矿石中还原出来 | |
| B. | 活泼金属Na用电解法冶炼 | |
| C. | 汞的冶炼只能用热分解法 | |
| D. | 铝的冶炼一般用热还原法 |
4.下列物质中,不能使酸性KMnO4溶液褪色的物质是( )
① ②乙烯 ③CH3COOH ④CH3CH2OH ⑤CH2=CH-CH3 ⑥
②乙烯 ③CH3COOH ④CH3CH2OH ⑤CH2=CH-CH3 ⑥
①
 ②乙烯 ③CH3COOH ④CH3CH2OH ⑤CH2=CH-CH3 ⑥
②乙烯 ③CH3COOH ④CH3CH2OH ⑤CH2=CH-CH3 ⑥
| A. | ①⑥ | B. | ①③④⑥ | C. | ①④ | D. | ①③⑥ |
11.一定温度下,可逆反应3X(g)+Y(g)?2Z(g)达到限度的标志是( )
| A. | 单位时间内生成3n mol X,同时消耗n mol Y | |
| B. | X全部生成Z | |
| C. | X、Y、Z的浓度相等 | |
| D. | X、Y、Z的分子数之比为3:1:2 |
1.下列有机化学方程式书写正确的是( )
| A. | CH4+Cl2$\stackrel{光照}{→}$CH2Cl2+H2 | |
| B. |  +HO-NO2$→_{△}^{浓硫酸}$ +HO-NO2$→_{△}^{浓硫酸}$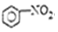 +H2O +H2O | |
| C. | H2C=CH2+Br2→CH3CHBr2 | |
| D. | CH3CH2OH+CH3COOH$→_{△}^{浓硫酸}$CH3COOCH2CH3 |
8.关于1.0mol/L醋酸和0.1mol/L醋酸的说法正确的是( )
| A. | 相同条件下二者与锌粉反应,前者速度慢 | |
| B. | 稀释相同体积时前者c(H+)大 | |
| C. | 等体积的两种醋酸与足量的锌粉反应,产生的H2体积比为10:1 | |
| D. | 相同条件下二者的电离程度相同 |
5.己烯雌酚(结构简式如下图所示),是一种激素类药物.下列叙述不正确的是( )


| A. | 己烯雌酚的分子式为C18H20O2 | |
| B. | 己烯雌酚与NaOH溶液、NaHCO3溶液均能反应 | |
| C. | 1mol己烯雌酚最多能与2mol Na发生反应 | |
| D. | 己烯雌酚与饱和溴水可以发生加成反应和取代反应 |
4.今有一包铁粉和铜粉混合粉末,为确定其组成,现提供4mol/L的FeCl3溶液(其他用品略),某合作学习小组同学的实验结果如下(假定反应前后溶液体积不变)( )
| 组别 | ① | ② | ③ | ④ |
| V[FeCl3(aq)]/mL | 100 | 100 | 100 | 100 |
| 混合粉末质量/g | 6 | 13.2 | 24 | 36 |
| 反应后剩余固体质量/g | 0 | 1.28 | 12.8 | 24.8 |
| A. | 第①组溶液中c(Fe3+)=3.0 mol/L | |
| B. | 第②组剩余固体是铜铁混合物 | |
| C. | 第④组反应后的滤液中c(Fe2+)=6 mol/L | |
| D. | 原混合粉末中n(Fe):n(Cu)=3:2 |
