题目内容
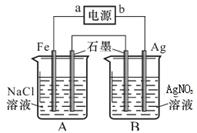
某同学设计出如下装置成功的证明了Cu和Ag的金属活动性顺序。请你原电池原理和实验装置,完成下列实验报告。

实验目的:探究Cu和Ag的金属活动性顺序
(1)电极材料:正极: ;负极: ;
硝酸银溶液的作用是 。
(2)写出电极反应式:
正极: ;负极: 。
(3)实验现象: 。
(4)实验结论: 。

实验目的:探究Cu和Ag的金属活动性顺序
(1)电极材料:正极: ;负极: ;
硝酸银溶液的作用是 。
(2)写出电极反应式:
正极: ;负极: 。
(3)实验现象: 。
(4)实验结论: 。
(12分)(1)银片(1分)、铜片(1分);参与氧化还原反应和导电(2分)
(2)正极:2Ag+ + 2e- =2Ag(2分),负极:Cu–2e- =Cu2+(2分)
(3)负极不断溶解,正极上有银白色固体析出,溶液由无色变为蓝色(2分)
(4)金属活动性Cu>Ag(2分)
(2)正极:2Ag+ + 2e- =2Ag(2分),负极:Cu–2e- =Cu2+(2分)
(3)负极不断溶解,正极上有银白色固体析出,溶液由无色变为蓝色(2分)
(4)金属活动性Cu>Ag(2分)
试题分析:(1)原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。铜比银活泼,所以铜是负极,银是正极,硝酸银溶液是电解质溶液,参与氧化还原反应和导电作用。
(2)负极是铜失去电子,电极反应式是Cu–2e- =Cu2+;正极是溶液中的银离子得到电子,则电极反应式是2Ag+ + 2e- =2Ag。
(3)根据以上分析可知,实验现象是负极不断溶解,正极上有银白色固体析出,溶液由无色变为蓝色。
(4)根据实验现象和原理可得出的结论是金属活动性Cu>Ag。
点评:该题是高考中的常见题型,属于基础性试题的考查。只要是考查学生对原电池工作原理的熟悉掌握程度,以及灵活运用知识解决实际问题的能量,有利于培养学生的逻辑推理能力,也有助于提高学生的应试能力和学习效率。

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
 只向PbO2极移动
只向PbO2极移动