题目内容
19.某溶液中只有Na+、CH3COO-、H+、OH-四种离子,且浓度大小的顺序为:c(CH3COO-)>c(Na+)>c(H+)>c(OH-),该溶液可能是( )| A. | 由0.1mol•L-1的CH3COOH溶液与0.1 mol•L-1的NaOH溶液等体积混合而成 | |
| B. | 由10mLpH=3的CH3COOH溶液与1 mL pH=11的NaOH溶液混合而成 | |
| C. | 由0.1mol•L-1的CH3COONa溶液与0.1 mol•L-1的NaOH溶液等体积混合而成 | |
| D. | 由0.1mol•L-1的CH3COONa溶液与0.1 mol•L-1的CH3COOH溶液等体积混合而成 |
分析 某溶液中只含有Na+、CH3COO-、H+、OH-四种离子,则溶液可能为醋酸钠溶液或醋酸钠与醋酸的混合溶液或醋酸钠与氢氧化钠的混合溶液,
再根据离子浓度大小顺序为c(CH3COO-)>c(Na+)>c(H+)>c(OH-),溶液显酸性,则不能为醋酸钠溶液,不能为醋酸钠与氢氧化钠的混合溶液,则溶液为醋酸钠与醋酸的混合溶液.
解答 解:A、由0.1mol•L-1的CH3COOH溶液与0.1 mol•L-1的NaOH溶液等体积混合,生成CH3COONa,溶液显碱性,已知溶液显酸性,则不能为醋酸钠溶液,故A错误;
B、由10mLpH=3的CH3COOH溶液与1 mL pH=11的NaOH溶液混合而成,醋酸过量,溶液中钠离子浓度较小,则c(CH3COO-)>c(H+)>c(Na+)>c(OH-),故B错误;
C、CH3COONa和NaOH的混合溶液显碱性,则c(OH-)>c(H+),且c(Na+)>c(CH3COO-),故C错误;
D、由0.1mol•L-1的CH3COONa溶液与0.1 mol•L-1的CH3COOH溶液等体积混合,溶液中醋酸的电离大于醋酸根离子的水解,溶液显酸性,则c(CH3COO-)>c(Na+)>c(H+)>c(OH-),故D正确;
故选D.
点评 本题考查了弱电解质的电离和盐的水解,考查学生利用溶液中的离子即离子的浓度关系来分析溶液中的溶质,然后利用电离和水解的知识来解答即可,题目难度中等.

练习册系列答案
相关题目
14.下列离子在溶液中可以大量共存的一组是( )
| A. | Mg2+、Na+、Cl-、OH- | B. | Na+、Ca2+、NO3-、CO32- | ||
| C. | K+、H+、Na+、HCO3- | D. | Na+、K+、NO3-、Cl- |
4.关于SO2的叙述中,正确的是( )
| A. | SO2的摩尔质量是64g | |
| B. | 1molSO2中所含分子数约为6.02×1023 | |
| C. | 1molSO2的质量是64g/mol | |
| D. | 常温常压下,1mol SO2的体积为22.4L |
11.下列各项中所述的两个量,前者一定大于后者的是( )
| A. | 25℃,将pH=4的盐酸和醋酸分别加水稀释成pH=5,所加水的量 | |
| B. | 25℃,pH=10的NaOH溶液和Na2CO3溶液中,由水电离出的c(OH-) | |
| C. | 25℃,物质的量浓度相等的 (NH4)2SO4和 (NH4)2CO3溶液中的c(NH4+) | |
| D. | 25℃,Na2CO3溶液中HCO3-和OH-的数目 |
8.在一定条件下,反应N2+3H2?2NH3 在2L密闭容器中进行,10min时NH3的质量增加了3.4g,则反应速率为( )
| A. | υ(H2)=0.02 mol/(L•min) | B. | υ(N2)=0.02 mol/(L•min) | ||
| C. | υ(NH3)=0.01 mol/(L•min) | D. | υ(N2)=0.01 mol/(L•min) |
9.医院里用HgCl2的稀溶液用作手术刀的消毒剂,HgCl2熔融时不导电,熔点低.HgCl2难溶于水,易溶于氯化钠饱和溶液中,关于HgCl2的描述不合理的是( )
| A. | 难溶的共价化合物 | B. | 是离子化合物 | ||
| C. | 是一种强电解质 | D. | 具有较强氧化性 |
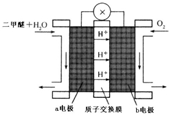 二甲醚(CH3OCH3)被称为21世纪的新型燃料,在未来可能替代汽油、液化气、煤气等并具有优良的环保性能.工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
二甲醚(CH3OCH3)被称为21世纪的新型燃料,在未来可能替代汽油、液化气、煤气等并具有优良的环保性能.工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应: HCO3-+OH-(用离子方程式表示);
HCO3-+OH-(用离子方程式表示);