题目内容
常温下现有的四份溶液:
①0.01 mol/L HCl;②0.01 mol/L CH3COOH;③pH=12 的氨水;④pH=12的NaOH溶液。
下列说法正确的是
①0.01 mol/L HCl;②0.01 mol/L CH3COOH;③pH=12 的氨水;④pH=12的NaOH溶液。
下列说法正确的是
| A.②中由水电离出的c(H+)=1×10-12mol/L |
| B.将①、③混合,若有pH=7,则消耗溶液的体积:③>① |
| C.将②、④等体积混合(体积变化忽略不计),则c(CH3COO-)+c(CH3COOH)=0.01 mol/L |
| D.将四份溶液均稀释10倍后溶液pH:③>④,②<① |
D
由于CH3COOH为弱电解质,故0.01 mol/L CH3COOH溶液中的c(H+)≠1×10-2mol/L,故由水电离出的c(H+)≠1×10-12mol/L,A项错误;因pH=12的氨水中氨水的浓度远大于0.01 mol/L,0.01 mol/L HCl与pH=12的氨水混合,当pH=7时,消耗溶液的体积:③<①,B项错误;将②、④等体积混合,溶液的总体积增大,c(CH3COO-)+c(CH3COOH)<0.01 mol/L,C项错误。0.01 mol/L HCl稀释10倍后pH=3。CH3COOH是弱酸稀释电离平衡右移,所以0.01 mol/L的CH3COOH稀释10倍后pH<3,D项正确。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
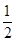 O2(g)═CO(g)△H1=-110.5kJ/mol
O2(g)═CO(g)△H1=-110.5kJ/mol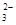
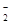
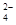
 +c(Z-)+c(OH-)
+c(Z-)+c(OH-)