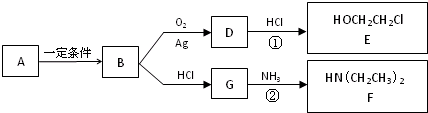
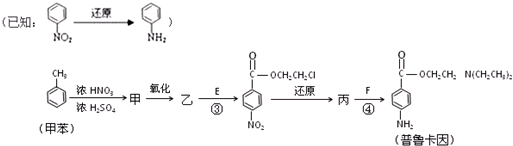
题目内容
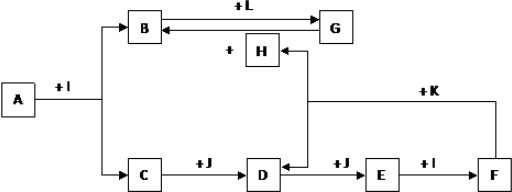
A、B、C、D、E为五种元素的单质,其余为化合物.其中只有E为金属元素,五种元素的原子序数按B、D、C、A、E顺序依次增大,D、C元素在周期表中位置相邻,在一定条件下,B分别和A、C、D化合生成甲、乙、丙,乙、丙每个分子中均含有10个电子;C和D化合可得丁.各物质相互转化关系如图:
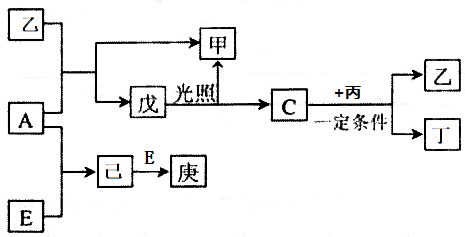
请回答下列问题:
(1)写出E元素在周期表的位置 .
(2)戊的名称为 ;用途 (只写一种).
(3)写出实验室制取A反应的离子方程式 .
(4)常温下A与足量的丙发生反应生成单质D,写出该反应的化学方程式 .
(5)写出足量E和稀硝酸反应的化学方程式: .
(6)实验室配制庚溶液的方法是 .

请回答下列问题:
(1)写出E元素在周期表的位置
(2)戊的名称为
(3)写出实验室制取A反应的离子方程式
(4)常温下A与足量的丙发生反应生成单质D,写出该反应的化学方程式
(5)写出足量E和稀硝酸反应的化学方程式:
(6)实验室配制庚溶液的方法是
考点:无机物的推断
专题:推断题
分析:B可以分别和C、D化合生成乙、丙,且乙、丙每个分子中均含有10个电子,乙、丙都含有氢元素,由于乙、丙为二元化合物,故B为氢气;D、C元素在周期表中位置相邻,由转化关系中,C与氢化物丙可以反应,则C为氧气,故乙为水;原子序数D<C,则D为氮气、丙为NH3,C和D化合可得丁为NO;B和A化合生成甲为氢化物,由转化关系中A与水反应得到化合物甲、戊,戊在光照分解得到甲与氧气,考虑戊为HClO,则A为Cl2、甲为HCl,E为金属与氯气反应生成己,己与E反应生成庚,E为变价金属,则E为Fe、己为FeCl3,庚为FeCl2,据此解答.
解答:
解:B可以分别和C、D化合生成乙、丙,且乙、丙每个分子中均含有10个电子,乙、丙都含有氢元素,由于乙、丙为二元化合物,故B为氢气;D、C元素在周期表中位置相邻,由转化关系中,C与氢化物丙可以反应,则C为氧气,故乙为水;原子序数D<C,则D为氮气、丙为NH3,C和D化合可得丁为NO;B和A化合生成甲为氢化物,由转化关系中A与水反应得到化合物甲、戊,戊在光照分解得到甲与氧气,考虑戊为HClO,则A为Cl2、甲为HCl,E为金属与氯气反应生成己,己与E反应生成庚,E为变价金属,则E为Fe、己为FeCl3,庚为FeCl2,
(1)E为Fe元素,在周期表的位置为:第四周期第Ⅷ族,
故答案为:第四周期第Ⅷ族;
(2)戊为HClO,其名称为:次氯酸,其用途:可以做漂白剂等,
故答案为:次氯酸;做漂白剂;
(3)实验室制取A(氯气)反应的离子方程式为:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O,
故答案为:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O;
(4)常温下A与足量的丙发生反应生成单质D,该反应的化学方程式:3Cl2+8NH3=N2+6NH4Cl,
故答案为:3Cl2+8NH3=N2+6NH4Cl;
(5)足量E和稀硝酸反应的化学方程式:3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O,
故答案为:3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O;
(6)实验室配制氯化亚铁溶液,要加入盐酸防止水解,加入铁粉防止氧化,具体实验方法是:向盐酸中加入适量的FeCl2晶体,搅拌溶解,然后加水稀释,并加入少许铁粉,
故答案为:向盐酸中加入适量的FeCl2晶体,搅拌溶解,然后加水稀释,并加入少许铁粉.
(1)E为Fe元素,在周期表的位置为:第四周期第Ⅷ族,
故答案为:第四周期第Ⅷ族;
(2)戊为HClO,其名称为:次氯酸,其用途:可以做漂白剂等,
故答案为:次氯酸;做漂白剂;
(3)实验室制取A(氯气)反应的离子方程式为:MnO2+4H++2Cl-
| ||
故答案为:MnO2+4H++2Cl-
| ||
(4)常温下A与足量的丙发生反应生成单质D,该反应的化学方程式:3Cl2+8NH3=N2+6NH4Cl,
故答案为:3Cl2+8NH3=N2+6NH4Cl;
(5)足量E和稀硝酸反应的化学方程式:3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O,
故答案为:3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O;
(6)实验室配制氯化亚铁溶液,要加入盐酸防止水解,加入铁粉防止氧化,具体实验方法是:向盐酸中加入适量的FeCl2晶体,搅拌溶解,然后加水稀释,并加入少许铁粉,
故答案为:向盐酸中加入适量的FeCl2晶体,搅拌溶解,然后加水稀释,并加入少许铁粉.
点评:本题考查无机物推断,乙、丙为10电子物质是推断突破口,对学生的逻辑推理有一定的要求,需要学生熟练掌握元素化合物知识,难度较大,(6)中注意铁盐、亚铁盐溶液的配制.

练习册系列答案
相关题目
下列说法正确的是( )
| A、光导纤维的材料是晶体硅 |
| B、金属越活泼,发现和使用的年代越早 |
| C、合理使用化肥有利于提高农作物产量 |
| D、高毒、高效、高残留化合物可用作未来粮食生产的杀虫剂 |
下列有关溶液中离子浓度的关系,不正确的是( )
| A、NaHC03溶液中存在:c(OH-)=c(H2CO3)+c(H+) |
| B、常温下,pH=3的盐酸和pH=ll的氨水等体积混合后,溶液中:c(NH4+)>c(Cl-) |
| C、0.2mol/L NH4Cl溶液与0.1mol/L NaOH溶液等体积混合后,溶液中:c(NH4+)>c(Na+) |
| D、相同温度下,0.2mol/L的CH3COOH溶液中c(H+)小于0.1mol/L的CH3COOH中c(H+)的两倍 |
下列离子反应方程式中,属于水解反应的是( )
| A、CN-+H2O?HCN+OH- |
| B、NH3?H2O?NH4++OH- |
| C、HCO3-+H2O?H3O++CO32- |
| D、H2CO3?HCO3-+H+ |
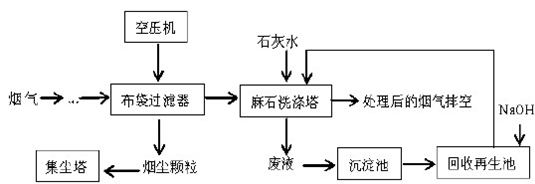
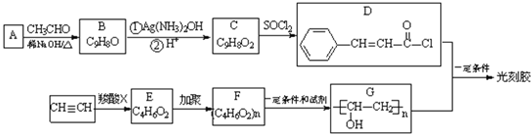
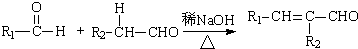 (R,R′为烃基或氢)
(R,R′为烃基或氢) (R,R′为烃基)
(R,R′为烃基)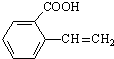 、
、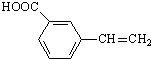 、
、
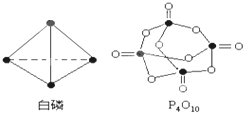 白磷(P4)是正四面体构型的分子,当与氧气作用形成P4O10时,每两个磷原子之间插入一个氧原子,此外,每个磷原子又以双键结合一个氧原子.如图:
白磷(P4)是正四面体构型的分子,当与氧气作用形成P4O10时,每两个磷原子之间插入一个氧原子,此外,每个磷原子又以双键结合一个氧原子.如图: