题目内容
【题目】如图各有机物相互转化关系中,无色气体A为石油裂解的产品之一,A的产量可以用来衡量一个国家石油化工水平,B、D均为日常生活中常见的有机物。
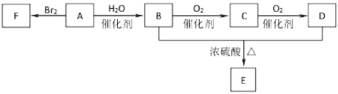
回答下列问题:
(1)由F生成乙二醇的反应条件为_________________________________________。
(2)A生成B的反应方程式为_______________________________________,B生成C的反应方程式为___________________________。
【答案】氢氧化钠的水溶液、加热 CH2=CH2+H2O ![]() CH3CH2OH 2CH3CH2OH+O2
CH3CH2OH 2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
【解析】
A的产量可以用来衡量一个国家石油化工水平,所以A为CH2=CH2,乙烯与溴发生加成反应生成F为CH2BrCH2Br,与水催化加成生成B为CH3CH2OH,乙醇被催化氧化生成C为CH3CHO,乙醛被催化氧化生成D为CH3COOH,CH3CH2OH和CH3COOH发生酯化反应生成E为CH3COOCH2CH3。
(1)F为CH2BrCH2Br,在氢氧化钠水溶液、加热的条件下发生水解生成乙二醇;
(2)A生成B为乙烯和水的加成反应,方程式为CH2=CH2+H2O![]() CH3CH2OH;
CH3CH2OH;
乙醇被催化氧化生成乙醛,方程式为2CH3CH2OH+O2![]() 2CH3CHO+2H2O。
2CH3CHO+2H2O。

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案【题目】某同学用已知物质的量浓度的NaOH测定未知物质的量浓度的盐酸,将20.00 ![]() 待测盐酸放入锥形瓶中,并滴加2-3滴酚酞作指示剂,用NaOH标准溶液进行滴定。重复上述滴定操作2-3次,记录数据如下。
待测盐酸放入锥形瓶中,并滴加2-3滴酚酞作指示剂,用NaOH标准溶液进行滴定。重复上述滴定操作2-3次,记录数据如下。
实验编号 |
| 滴定完成时, | 待测盐酸的体积/ |
1 | 0.10 | 22.62 | 20.00 |
2 | 0.10 | 22.72 | 20.00 |
3 | 0.10 | 22.80 | 20.00 |
① 滴定达到终点的标志是____________________________。
② 根据上述数据,可计算出该盐酸的浓度约为_______(保留两位有效数字)。
③ 排除碱式滴定管中气泡的方法应采用如图所示操作中的________,然后轻轻挤压玻璃球使尖嘴部分充满碱液。

④ 在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有________(填字母序号)。
A. 滴定终点读数时俯视
B. 酸式滴定管使用前,水洗后未用待测盐酸润洗
C. 锥形瓶水洗后未干燥
D. 称量的![]() 固体中混有
固体中混有![]() 固体
固体
E. 碱式滴定管尖嘴部分有气泡,滴定后消失