��Ŀ����
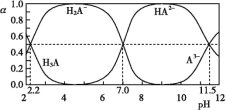
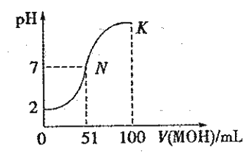
����Ŀ��������Ԫ��a��b��c��d��ԭ��������������a��cλ��ͬ���壬b��dλ��ͬ���壬cΪ������Ԫ����ԭ�Ӱ뾶����ԭ�ӡ�X��Y���ֻ��������������Ԫ�أ������£�0.1 mol��L��1 Y��Һ��c(H+)=0.1mol/L����X��Һ�еμ�Y��Һ��������������ʵ���������Y��Һ��Y�����ʵ����Ĺ�ϵ��ͼ��ʾ(������Һ������ȫ���ݳ�)������˵����ȷ����(����)

A.�����Ӱ뾶��d>c>b
B.��̬�⻯������ȶ��ԣ�d>b
C.c2b2�к����ֻ�ѧ��
D.X��Y��Һ�еμ��Ȼ�����Һ���������ɫ����
���𰸡�C
��������
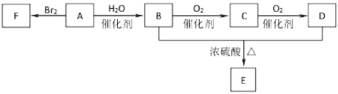
�����⼰��ͼ֪��Y���������ƣ�XΪ���������ƣ����߷����ķ�ӦΪNaHSO3��NaHSO4=Na2SO4��SO2����H2O����aΪ�⣬bΪ����cΪ�ƣ�dΪ��
A. �����Ӱ뾶��r(S2��)>r(O2��)>r(Na��)����A����
B. H2O�����ȶ��Ա�H2Sǿ����B����
C. Na2O2�к������Ӽ����Ǽ��Թ��ۼ�����C��ȷ��
D. NaHSO3�����Ȼ�����������ɫ��������D����
��ѡC��

��ϰ��ϵ�д�
 ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д� ͬ����չ�Ķ�ϵ�д�
ͬ����չ�Ķ�ϵ�д�
�����Ŀ