题目内容
【题目】向含有MgCO3固体的溶液中滴加少许浓盐酸(忽略体积变化),下列数值变小的是
A.c(CO32- ) B.c(Mg2+) C.c(H+) D.Ksp(MgCO3)
【答案】A
【解析】
试题分析:MgCO3固体的溶液中存在溶解平衡:MgCO3(s)Mg2+(aq)+CO32-(aq),加入少量稀盐酸可与CO32-促使溶解平衡正向移动,故溶液中c(CO32-)减小,c(Mg2+)及c(H+)增大,Ksp(MgCO3)只与温度有关,不变,只有A正确;故选A。

【题目】X、Y、Z、W为四种短周期元素,其中Y元素原子核外最外层电子数是其电子层数的3倍,它们在周期表中的相对位置如下图所示:
X | Y | |
Z | W |
请回答下列问题:
(1)W位于周期表中第__________周期,第____族;
(2)X可形成双原子分子,其分子的电子式是_____;Y和氢元素形成的10电子微粒中常见+1价阳离子为_____(填化学式,下同);Z和氢元素形成的18电子微粒中常见的-1价阴离子为______;
(3)工业上将干燥的W单质通入熔融的Z单质中可制得化合物Z2W2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,写出Z2W2与水反应的化学方程式______________________。
(4)在一定条件下,由元素Y和Z组成的一种气态化合物可发生催化氧化反应,反应达平衡时有三种气态物质共存,已知每转移4mol电子放热190.0kJ,该反应的热化学方程式是_____________。
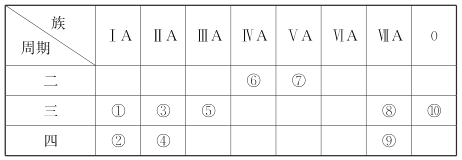
【题目】下表是元素周期表的一部分,针对表中的①~⑩种元素,回答下列问题:
主族 周期 | I A | II A | III A | IV A | V A | VI A | VII A | 0族 |
2 | ① | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
4 | ⑨ | ⑩ |
(1)元素①的名称是_____________;比元素⑧质子数多10的元素在周期表中所处位置___________。
(2)元素③的单质的电子式为_____________,元素③的气态氢化物与其最高价氧化物的水化物反应的化学方程式为_________________________________________。
(3)用电子式表示元素⑨与⑥的化合物的形成过程:____________________________,该化合物属于__________(填“共价或“离子”)化合物。
(4)表示②与⑦形成的化合物的电子式:________________________,该化合物是由__________(填“极性”或“非极性”)键形成的。
(5)元素⑥的氢化物的结构式为_____________________;该氢化物常温下和元素⑦的单质反应的化学方程式为________________________________;元素③④⑥形成的氢化物沸点由高到底的顺序(写化学式)___________________________。
(6)④、⑥、⑦、⑨四种元素形成的简单离子,离子半径由大到小的顺序是(写离子符号)__________________________________。
(7)某原子有6个电子、7个中子,写出其元素符号:________________________。
(8)④⑥可与氢元素构成多种10电子和18电子的粒子,其中符合下列要求的粒子的电子式为:4核18电子的分子_____________________,10电子的阳离子_______________________________。