题目内容
【题目】下表是元素周期表示意图的一部分。
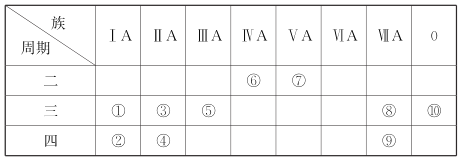
请回答下列问题:
(1)元素③~⑦中,原子半径最大的是____(填元素符号)。
(2)元素①~⑩中,最高价氧化物对应的水化物中酸性最强的是____(填化学式,下同),呈两性的氢氧化物是____。
(3)元素⑦的最高价氧化物对应的水化物与其氢化物能生成盐M,M中含有的化学键类型有__________。
【答案】 Ca HClO4 Al(OH)3 离子键、共价键
【解析】根据元素在元素周期表中的相对位置可知①~⑩分别是Na、K、Mg、Ca、Al、C、N、Cl、Br、Ar。
(1)同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,因此元素③~⑦中,原子半径最大的是Ca。(2)元素①~⑩中非金属性最强的是Cl,最高价氧化物对应的水化物中酸性最强的是HClO4,呈两性的氢氧化物是Al(OH)3。(3)元素⑦的最高价氧化物对应的水化物与其氢化物能生成盐M,M是硝酸铵,其中含有的化学键类型有离子键、共价键。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目