题目内容
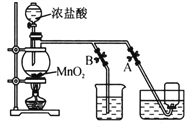
【题目】碳酸钴常用作电子材料、磁性材料的添加剂,受热时可分解生成三种氧化物。为了确定其组成,某化学兴趣小组同学设计了如图所示的装置进行实验。
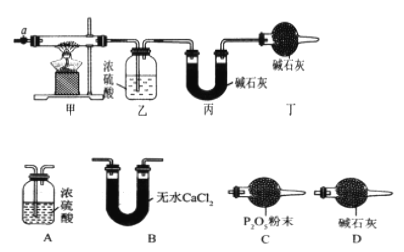
(1)请完成下列实验步骤:
①称取 3. 65 g 样品置于硬质玻璃管内,称量乙、丙装置的质量;
②按如图所示装置组装好仪器,并检验装置气密性;
③加热甲中玻璃管,当乙装置中_______ (填实验现象),停止加热;
④打开活塞 a,缓缓通入空气数分钟后,称量乙、丙装置的质量;
⑤计算。
(2)步骤④中缓缓通入空气数分钟的目的是___________________________________。
(3)某同学认为上述实验装置中存在一个明显缺陷,为解决这一问题,可选用下列装置中的_______(填字母)连接在_______(填装置连接位置)。
(4)若按正确装置进行实验,测得如下数据。
乙装置的质量/g | 丙装置的质量/g | |
加热前 | 80.00 | 62.00 |
加热后 | 80.36 | 62.88 |
则该碱式碳酸钴的化学式为______________。
【答案】 ③中不再有气泡产生 将装置中产生的CO2 和H2O全部排入乙丙装置中 D 活塞a前(或装置甲前) Co3(OH)4(CO3)2
【解析】(1)③加热甲中玻璃管,当乙装置中不再有气泡产生,即碱式碳酸钴分解完毕;
(2)步骤④中缓缓通入空气数分钟,将装置中生成的CO2和H2O全部排入乙、丙装置中,以免影响测量结果;
(3)在活塞a前,加装装置D,装置中盛放的碱石灰容易吸收空气中的水蒸气和二氧化碳,故可选用下列装置中的D,且连接在活塞a前(或装置甲前);
(4)碱式碳酸钴样品3.65g,反应前乙装置的质量为80.00g,反应后质量为80.36g,故生成水的质量为80.36g-80.00g=0.36g,物质的量为![]() =0.02mol;反应前丙装置的质量为62.00g,反应后质量为62.88g,生成二氧化碳的质量为62.88g-62.00g=0.88g,物质的量为
=0.02mol;反应前丙装置的质量为62.00g,反应后质量为62.88g,生成二氧化碳的质量为62.88g-62.00g=0.88g,物质的量为![]() =0.02mol,故Co的质量为3.65g-0.02mol×2×17g/mol-0.02mol×60g/mol=1.77g,故Co原子物质的量为:
=0.02mol,故Co的质量为3.65g-0.02mol×2×17g/mol-0.02mol×60g/mol=1.77g,故Co原子物质的量为: ![]() =0.03mol,根据Co、H、C元素守恒可知,x:y:z=0.03mol:0.02mol×2:0.02mol=3:4:2,故碱式碳酸钴的化学式为Co3(OH)4(CO3)2。
=0.03mol,根据Co、H、C元素守恒可知,x:y:z=0.03mol:0.02mol×2:0.02mol=3:4:2,故碱式碳酸钴的化学式为Co3(OH)4(CO3)2。

 阅读快车系列答案
阅读快车系列答案