题目内容
13.下列说法错误的是( )| A. | 配制一定物质的量浓度的NaCl溶液定容时,俯视会使溶液浓度偏大 | |
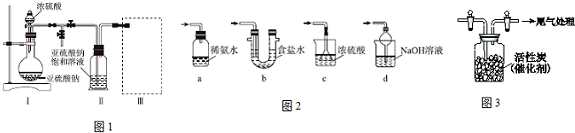
| B. | 除去氯气中HCl用饱和食盐水 | |
| C. | 海水开发用的部分过程如图:工业生产中常选用NaOH作为沉淀剂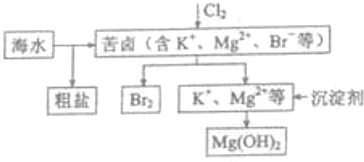 | |
| D. | 富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收 |
分析 A、定容时俯视刻度线,导致配制的溶液的体积偏小,溶液未达到刻度线;
B、饱和氯化钠溶液中氯气溶解度减小,氯化氢极易溶于水;
C、工业生产一般用生石灰或石灰水作沉淀剂;
D、先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收转化为HBr,达到富集的目的.
解答 解:A、配制一定物质的量浓度的NaCl溶液定容时,俯视溶液未达到刻度线,会使溶液浓度偏大,故A正确;
B、HCl易溶于水,而氯气不溶于或难溶于饱和食盐水,可用于除杂,故B正确;
C、氢氧化钠是强碱,具有强腐蚀性、价格高,工业生产一般用生石灰或石灰水作沉淀剂,故C错误;
D、海水提取溴一般用氯气置换溴离子转化为溴单质,用空气和水蒸气吹出单质溴,再用SO2将其还原吸收转化为HBr,达到富集的目的,故D正确,
故选C.
点评 本题考查海水资源的综合利用,注意掌握中学常见的化学工业,侧重对化学与技术的考查,掌握基础是关键,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.下列实验不能达到目的是( )
| A. | 向25mL沸水中滴加5-6滴稀的FeCl3溶液制备氢氧化铁胶体 | |
| B. | 只用少量水就可鉴别Na2CO3和NaHCO3固体 | |
| C. | 用FeSO4、NaOH和盐酸等试剂在空气中可以制备较纯净的FeCl3溶液 | |
| D. | 用NaOH溶液和盐酸可除去MgCl2溶液中混有的AlCl3 |
4.1mol H2SO4中氧原子数( )
| A. | 1 mol | B. | 2 mol | C. | 3 mol | D. | 4 mol |
1.在四种不同条件下测得反应2SO2+O2?2SO3的反应速如表所示:
其中反应速率最快的是( )
| 编号 | (1) | (2) | (3) | (4) |
| 反应速率[mol/(L.s)] | v(SO2) | v(O2) | v(SO3) | v(O2) |
| 0.4 | 0.25 | 0.5 | 0.3 |
| A. | (1) | B. | (2) | C. | (3) | D. | (4) |
8.下列离子方程式正确的是( )
| A. | 澄清的石灰水与稀盐酸反应Ca(OH)2+2H+═Ca2++2H2O | |
| B. | 铁与盐酸的反应 Fe+2H+═Fe3++H2↑ | |
| C. | 铜片插入硝酸银溶液中Cu+Ag+═Cu2++Ag | |
| D. | 纯碱和稀盐酸反应 CO32-+2H+═CO2↑+H2O |
18.下列说法中正确的是( )
| A. | 氨能在空气中燃烧,生成N2和水 | |
| B. | NO2溶于水生成HNO3,NO2属于酸性氧化物 | |
| C. | 所有的铵盐加热分解都能产生NH3 | |
| D. | 铜与浓硝酸反应时,硝酸既表现氧化性又表现酸性 |
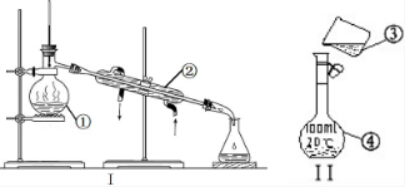 掌握仪器的名称、组装及使用方法是中学化学实验的基础,下图为两套实
掌握仪器的名称、组装及使用方法是中学化学实验的基础,下图为两套实