题目内容
1.在四种不同条件下测得反应2SO2+O2?2SO3的反应速如表所示:| 编号 | (1) | (2) | (3) | (4) |
| 反应速率[mol/(L.s)] | v(SO2) | v(O2) | v(SO3) | v(O2) |
| 0.4 | 0.25 | 0.5 | 0.3 |
| A. | (1) | B. | (2) | C. | (3) | D. | (4) |
分析 化学反应速率与其计量数之比的值越大,说明该反应速率越快,据此分析解答.
解答 解:(1)$\frac{v(S{O}_{2})}{2}$=$\frac{0.4}{2}$mol/(L.s)=0.2mol/(L.s);
(2)$\frac{v({O}_{2})}{1}$=$\frac{0.25}{1}$mol/(L.s)=0.25mol/(L.s);
(3)$\frac{v(S{O}_{3})}{2}$=$\frac{0.5}{2}$mol/(L.s)=0.25mol/(L.s);
(4)$\frac{v({O}_{2})}{1}$=$\frac{0.3}{1}$mol/(L.s)=0.3mol/(L.s);
反应速率最快的是(4),故选D.
点评 本题考查化学反应速率大小比较,侧重考查学生计算能力,反应速率大小比较可以将不同物质转化为同一物质判断,也可以根据反应速率与计量数比值大小判断,注意:比较反应速率大小时单位要统一.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
11.美、德两国成功合成具有化学特性的氢铝化合物(AlH3)n,关于氢铝化合物的推测不正确的是( )
| A. | 氢铝化合物与水反应生成氢氧化铝和氢气 | |
| B. | 氢铝化合物中铝显+3价,氢显-1价 | |
| C. | 铝与水蒸气高温下反应生成氢铝化合物 | |
| D. | 氢铝化合物具有强还原性 |
12.为提纯下列物质(括号内为杂质),选用的试剂或方法有错误的是( )
| 物质 | 试剂 | 分离方法 | |
| A | 硝酸钾(氯化钠 ) | 蒸馏水 | 降温结晶 |
| B | 氢氧化铁胶体(Fe3+) | 蒸馏水 | 渗析 |
| C | 甲烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| D | 乙醇(水) | 生石灰 | 蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
9.下列有关阿佛加德罗常数(NA)的说法错误的是( )
| A. | 22.4LO2所含的分子数目为NA | |
| B. | 0.5molH2O含有的原子数目为1.5NA | |
| C. | 7.8gmolNa2O2与H2O反应转移电子数目为0.1NA | |
| D. | 0.5NA个氯气分子的物质的量是0.5mol |
6.有关实验的叙述,正确的是( )
| A. | 配制一定物质的量浓度的溶液,定容时俯视会导致所配溶液浓度偏大 | |
| B. | 用玻璃棒蘸取溶液,点在湿润的pH试纸上测定溶液的pH值 | |
| C. | 用NaOH溶液洗涤并灼烧铂丝后,再进行焰色反应 | |
| D. | 用瓷坩埚熔融氢氧化钠或碳酸钠 |
13.下列说法错误的是( )
| A. | 配制一定物质的量浓度的NaCl溶液定容时,俯视会使溶液浓度偏大 | |
| B. | 除去氯气中HCl用饱和食盐水 | |
| C. | 海水开发用的部分过程如图:工业生产中常选用NaOH作为沉淀剂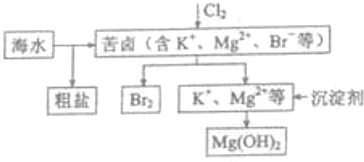 | |
| D. | 富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收 |
11.能够用键能的大小解释的是( )
| A. | 常温常压下,氯气呈气态而溴单质呈液态 | |
| B. | 硝酸是挥发性酸,硫酸是难挥发性的酸 | |
| C. | 稀有气体一般难发生化学反应 | |
| D. | 氮气在常温下很稳定,化学性质不活泼 |