题目内容
在一个体积可变的密闭容器中,通入2molHI气体,在一定条件下建立如下平衡:2HI(g) I2(g)+H2(g);△H>0,测得平衡时容器体积为1L,c(I2)=0.5mol/L。改变相关条件,下列结论正确的是
I2(g)+H2(g);△H>0,测得平衡时容器体积为1L,c(I2)=0.5mol/L。改变相关条件,下列结论正确的是
| A.保持容器体积不变,升高温度,混合气体的颜色逐渐变深 |
| B.恒温,恒容,充入一定量氦气(不参与反应),则正反应速率和逆反应速率均增大 |
| C.恒温,缓慢压缩容器,使容器体积恒定为0.2L,一定时间后,测得c(I2)=2.5mol/L |
| D.恒温、恒压,再通入2molHI气体,到达平衡状态后,HI转化率会提高 |
AC
解析试题分析:A、正反应吸热,升高温度,平衡向正反应方向移动,混合气体的颜色逐渐变深,故A正确;B、保持容器体积与温度不变,充入一定量氦气,反应物的浓度不变,速率不变,故B错误;C、反应前后气体的体积相等,改变压强平衡不移动,使容器体积恒定为0.2L,I2的物质的量不变,则c(I2)=0.5mol/L× =2.5mol/L,故C正确;D、保持容器压强和温度不变,再通入2molHI气体,在恒压条件下与原平衡状态相同,为等效平衡,则
=2.5mol/L,故C正确;D、保持容器压强和温度不变,再通入2molHI气体,在恒压条件下与原平衡状态相同,为等效平衡,则
2HI(g) I2(g)+H2(g)
I2(g)+H2(g)
起始:2mol 0 0
转化:1mol 0.5ml 0.5mol
平衡:1mol 0.5mol 0.5mol
HI的转化率为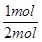 ×100%=50%,再通入2molHI气体,到达平衡状态后,HI的转化率应为50%,故D错误,故选AC。
×100%=50%,再通入2molHI气体,到达平衡状态后,HI的转化率应为50%,故D错误,故选AC。
考点:考查外界条件对平衡状态的影响以及有关计算

在一定温度下,将一定量的气体通入体积为2L的密闭容器中,使其发生反应,,有关物质X、Y、Z的物质的量的变化如图所示。则下列有关推断正确的是( ) 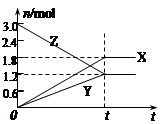
| A.该反应的化学方程式为: 3Z = 3X+2Y |
| B.t0时,X、Y、Z的质量不再改变 |
| C.t0时,Z的浓度为1.2 mol/L |
| D.t0时,反应停止,反应速率为0 |
一定条件下,在一恒容密闭容器中,能表示反应 X(g)+2Y(g) 2Z(g) 一定达到化学平衡状态的是
2Z(g) 一定达到化学平衡状态的是
①容器中气体的密度不再发生变化
②X、Y、Z的浓度不再发生变化
③容器中的压强不再发生变化
④单位时间内生成2n mol Z,同时消耗2n mol Y
| A.①② | B.②③ | C.③④ | D.①④ |
一定条件下将0.1 mol N2和0.3 mol H2置于密闭容器中发生反应N2+3H2 2NH3。下列关于该反应的说法正确的是
2NH3。下列关于该反应的说法正确的是
| A.最终可生成0.2 mol NH3 | B.使用催化剂不影响反应速率 |
| C.升高温度反应速率增大 | D.增大压强反应速率减小 |
下列有关说法正确的是
| A.反应SiO2(s)+ 3C(s) =" SiC(s)" + 2CO(g)室温下不能自发进行,则该反应的△H<0 |
| B.铅蓄电池放电过程中,正极质量增加,负极质量减小 |
C.25℃下,在NH3·H2O稀溶液中,加水, 的值不变 的值不变 |
| D.在NaHS溶液中,滴入少量CuCl2溶液产生黑色沉淀,HS-水解程度增大,pH增大 |
反应m A + n B  p C中,m、n、p为各物质的计量数。现测得C每分钟增加a mol/L,B每分钟减少1.5a mol/L,A每分钟减少0.5a mol/L,则m:n:p为
p C中,m、n、p为各物质的计量数。现测得C每分钟增加a mol/L,B每分钟减少1.5a mol/L,A每分钟减少0.5a mol/L,则m:n:p为
| A.2:3:1 | B.1:3:2 | C.2:3:3 | D.3:2:1 |
在相同条件下(T=500K),相同体积的甲乙两容器,甲中充入1gSO2和1gO2,乙中充入2gSO2和2gO2,下列叙述中不正确的是( )
| A.反应速率:乙>甲 | B.平衡混合物中SO2的体积分数:乙>甲 |
| C.SO2的转化率:乙>甲 | D.平衡时O2的浓度:乙>甲 |
向容积相同的甲、乙密闭容器中投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知N2(g) + 3H2(g)  2NH3(g) ΔH=-92.4 kJ·mol
2NH3(g) ΔH=-92.4 kJ·mol ):
):
| | 反应物投入量 | NH3的浓度 (mol·L  ) ) | 反应的 能量变化 | 体系压强 (Pa) | 反应物 转化率 |
| 甲 | 1mol N2、3mol H2 | c1 | 放出a kJ | p1 | α1 |
| 乙 | 2mol NH3 | c2 | 吸收b kJ | p2 | α2 |
下列说法正确的是( )
A.c1 = c2 B.a + b =" 1" C.p1>p2 D.α1 +α2>1
某温度时,在密闭容器中X、Y、Z三种气体浓度的变化如图甲所示,若其他条件不变,当温度分别为T1和T2时,Y的体积分数与时间关系如图乙所示。则下列结论正确的是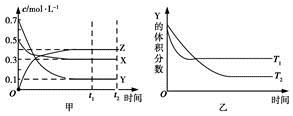
A.该反应的热化学方程式为X(g)+3Y(g)  2Z(g) ΔH>0 2Z(g) ΔH>0 |
| B.若其他条件不变,升高温度,正、逆反应速率均增大,X的转化率减小 |
| C.达到平衡后,若其他条件不变,减小容器体积,平衡向逆反应方向移动 |
| D.达到平衡后,若其他条件不变,通入稀有气体,平衡向正反应方向移动 |