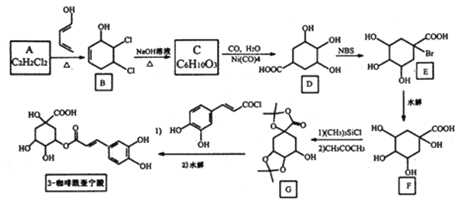
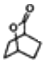
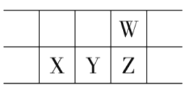
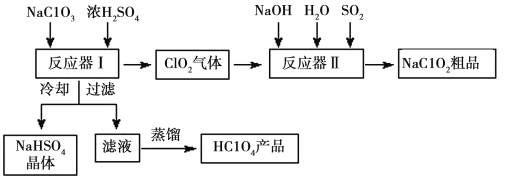
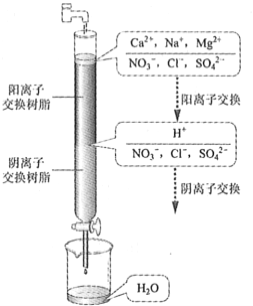
题目内容
【题目】常温下,下列各组离子在指定溶液中能大量共存的是( )
A.无色透明的溶液中:![]() 、
、![]() 、
、![]() 、
、![]()
B.![]() =1×10-12的溶液中:K+、
=1×10-12的溶液中:K+、![]() 、
、![]() 、
、![]()
C.![]() 的溶液中:
的溶液中:![]() 、
、![]() 、
、![]() 、
、![]()
D.能使甲基橙变红的溶液中:![]() 、
、![]() 、
、![]() 、
、![]()
【答案】B
【解析】
离子之间能够大量共存是指离子之间既不发生反应生成沉淀、气体、水、弱电解质等,也不发生氧化还原反应、络合反应等。
A. 含有Fe3+的溶液呈黄色,不符合无色条件,且Fe3+、SCN发生络合反应而不能大量共存,A项错误;
B. ![]() =1×10-12的溶液,呈碱性,这几种离子之间不反应且都不与氢氧根离子反应,所以能大量共存,B项正确;
=1×10-12的溶液,呈碱性,这几种离子之间不反应且都不与氢氧根离子反应,所以能大量共存,B项正确;
C. Fe2+、MnO4发生氧化还原反应而不能大量共存,C项错误;
D. 能使甲基橙溶液变红色,说明溶液呈酸性,HCO3能和氢离子反应生成二氧化碳和水而不能大量共存,D项错误;
答案选B。

【题目】化学反应伴随能量变化,获取反应能量变化有多条途径。
(1)下列反应中,属于吸热反应的是______(填字母)。
A.Na2O与水反应 B.甲烷的燃烧反应 C.CaCO3受热分解 D.锌与盐酸反应
(2)获取能量变化的途径
① 通过化学键的键能计算。已知:
化学键种类 | H—H | O=O | O—H |
键能(kJ/mol) | 436 | 498 | 463.4 |
计算可得:2H2(g)+ O2(g) =2H2O(g) H=____________kJ·mol-1
② 通过物质所含能量计算。已知反应中A+B=C+D中A、B、C、D所含能量依次可表示为E A、EB、 EC、 ED,该反应△H=_______。
③ 通过盖斯定律可计算。已知在25℃、101kPa时:
Ⅰ.2Na(s)+![]() O2 (g) =Na2O(s) △H=-414kJ·mol-1
O2 (g) =Na2O(s) △H=-414kJ·mol-1
Ⅱ.2Na(s)+O2(g) =Na2O2(s) △H=-511kJ·mol-1
写出Na2O2与Na反应生成Na2O的热化学方程式__________。
④利用实验装置测量。测量盐酸与NaOH溶液反应的热量变化的过程中,若取50 mL 0.50 mol·L-1的盐酸,则还需加入________(填序号)。
A.50 mL 0.50 mol·L-1 NaOH溶液
B.50 mL 0.55 mol·L-1NaOH溶液
C.1.0 g NaOH固体