��Ŀ����
���������ֳ�����ͬ�������壺��б�����������֪���³�ѹ�£�
�� S (s����б)+O2 (g)��SO2 (g)+297.16kJ��
�� S (s������)+O2 (g)��SO2 (g)+296.83kJ
����˵����ȷ����
�� S (s����б)+O2 (g)��SO2 (g)+297.16kJ��
�� S (s������)+O2 (g)��SO2 (g)+296.83kJ
����˵����ȷ����
| A�����³�ѹ�µ�б����������ȶ� |
B����б��ת��Ϊ������������仯������ͼ��ʾ |
| C��S(g)+O2(g)��SO2(g)+Q3 Q3>296.83kJ |
| D����Ӧ��������1 L SO2 (g)�ų�297.16kJ���� |
C
����������ɢ٢ڣ����ݸ�˹�����У�S (s����б)��S (s������)+0.33kJ��A������Խ��Խ�ȶ�����S�����������ȶ�������B���÷�ӦΪ���ȷ�Ӧ���ʷ�Ӧ������������������������������C���ӹ�̬�����������ȵģ��ʴ���̬��Ӧ���ų����������࣬��ȷ��D��Ӧ��Ϊ����1molSO2���ų���������

��ϰ��ϵ�д�
 ������ѧ���̲���ȫ���ϵ�д�
������ѧ���̲���ȫ���ϵ�д� ������ʱ����ҵ����ϵ�д�
������ʱ����ҵ����ϵ�д� ��ĩ���ƾ�ϵ�д�
��ĩ���ƾ�ϵ�д�
�����Ŀ


 4NO(g)+6H2O(g) ��H =" ��905" kJ/mol ������Ӧ
4NO(g)+6H2O(g) ��H =" ��905" kJ/mol ������Ӧ

 2NH3 (g) ��H<0��
2NH3 (g) ��H<0��


 2NH3(g)��H<0
2NH3(g)��H<0
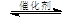 CH3OCH3(g) + 3H2O(g)
CH3OCH3(g) + 3H2O(g)