题目内容
1.某同学组装了如图所示的电化学装置,则下列说法正确的是( )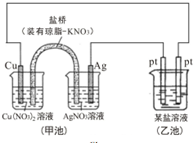
| A. | 实验过程中,甲池左侧烧杯中NO3-的浓度增大 | |
| B. | 图中甲池中的盐桥可以是装琼脂的饱和KCl溶液 | |
| C. | 若乙池为Na2SO4溶液,一段时间后,右边Pt极上产生了0.672L气体(标准状况),则甲池中Ag电极质量增加12.96g | |
| D. | Cu电极发生还原反应 |
分析 甲池为原电池装置,活泼的铜失电子作负极,电流方向从正极流向负极,负极上失电子发生氧化反应,正极上得电子发生还原反应,铜放电生成铜离子,盐桥中的阴离子硝酸根离子向左边移动,如果用铜制U形物代替“盐桥”,甲池中的右边一个池为原电池装置,以此解答该题.
解答 解:A.实验过程中,铜放电生成铜离子,盐桥中的阴离子硝酸根离子向左边移动,所以左侧烧杯中NO3-的浓度变大,故A正确;
B.正极所在的电解质溶液为硝酸银溶液,氯离子和银离反应,所以不可以用KCl饱和溶液制得的琼脂,故B错误;
C.若乙池为Na2SO4溶液,一段时间后,右边Pt极上产生了0.672L气体,应为氢气,且n(H2)=$\frac{0.672L}{22.4L/mol}$=0.03mol,由2H++2e-=H2↑可知转移0.06mol电子,由电极方程式Ag++e-=Ag可知生成0.06molAg,质量为0.06mol×108g/mol=6.48g,故C错误,
D.铜比银活泼,为原电池的负极,故D错误.
故选A.
点评 本题考查了原电池原理,正确判断正负极是解本题关键,再结合各个电极上发生的反应来分析解答,题目难度中等.

练习册系列答案
 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
11.已知aAn+、bB(n+1)+、cCn-、dD(n+1)-具有相同电子层结构,关于A、B、C、D四种元素的叙述正确的是( )
| A. | 气态氢化物的稳定性:D>C | |
| B. | 原子序数:b>a>c>d | |
| C. | 最高价氧化物对应水化物的碱性:B>A | |
| D. | 原子半径:B>A>D>C |
12.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 新制的氯水中:Ba2+、Fe2+、CO32- | |
| B. | 0.1 mol•L-1HNO3溶液中:Mg2+、SO42-、Cl- | |
| C. | 0.1 mol•L-1NH4Cl溶液中:K+、OH-、SO42- | |
| D. | 使石蕊变红色的溶液中:Na+、Cu2+、HCO3- |
9.有机物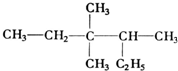 的正确命名为( )
的正确命名为( )
 的正确命名为( )
的正确命名为( )| A. | 2-乙基-3,3-二甲基-4-乙基戊烷 | B. | 3,3,4-三甲基已烷 | ||
| C. | 3,3-二甲基-4-乙基戊烷 | D. | 2,3,3-三甲基已烷 |
16.下列各组有机化合物中,不论两者以什么比例混合,只要总物质的量一定,则完全燃烧时生成的水的质量和消耗氧气的质量不变的是( )
| A. | C3H8,C4H6 | B. | C3H6,C3H8O | C. | C2H6,C4H6O2 | D. | CH4O,C3H4O5 |
6.取两份质量相等的有机物M,一份与足量的钠反应放出气体V1升,另一份与足量NaHCO3溶液反应放出气体V2升;若同温同压下V1=V2,则M是( )
| A. | HCOOH | B. | HOOC-COOH | C. | HOCH2CH2COOH | D. | HOC6H4OOCH |
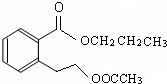 或
或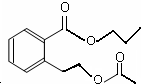 .
.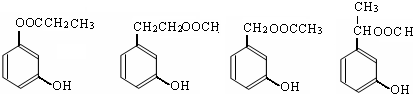 (任意两个).
(任意两个).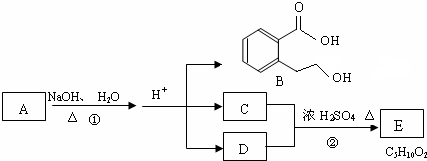
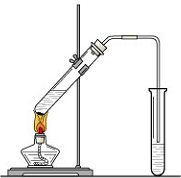 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置来制取乙酸乙酯.试回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置来制取乙酸乙酯.试回答下列问题: