题目内容
6.取两份质量相等的有机物M,一份与足量的钠反应放出气体V1升,另一份与足量NaHCO3溶液反应放出气体V2升;若同温同压下V1=V2,则M是( )| A. | HCOOH | B. | HOOC-COOH | C. | HOCH2CH2COOH | D. | HOC6H4OOCH |
分析 能与钠反应的有机物可能含有-OH、-COOH,或-OH和-COOH,能与NaHCO3溶液反应放出气体,有机物分子中含有-COOH;
质量相等的有机物M,物质的量相等,设物质的量为1mol,计算生成气体物质的量,相同条件下物质的量之比等于体积之比,结合生成气体体积判断.
解答 解:A.2HCOOH~H2 HCOOH~CO2,
1mol 0.5mol 1mol 1mol
所以生成气体的体积不相等,故A错误;
B.HOOC-COOH~H2 HOOC-COOH~CO2,
1mol 1mol 1mol 2mol
所以生成气体的体积不相等,故B错误;
C.HO(CH2)2COOH~H2 HO(CH2)2COOH~CO2
1mol 1mol 1mol 1mol
生成的气体体积相等,故C正确;
D.HOC6H4OOCH不碳酸氢钠反应,故D错误;
故选C.
点评 本题以化学计算为载体,考查官能团的结构性质,题目难度中等,注意掌握中学常见官能团的结构性质,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
相关题目
16.J、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如表所示.已知J元素最低负化合价的绝对值与其原子最外层电子数相等,M是地壳中含量最多的金属元素.下列说法错误的是( )
| J | ||
| R |
| A. | M和T组成的化合物是共价化合物 | |
| B. | M单质能与氢氧化钠溶液反应,产生一种可燃性气体 | |
| C. | R、T两元素的气态氢化物中,R的气态氢化物更稳定 | |
| D. | J、M、R、T元素最高价氧化物对应的水化物中酸性最强的是HTO4 |
17.下列有关反应的离子方程式正确的是( )
| A. | 二氧化碳与石灰水反应:CO2+2OH-═CO32-+H2O | |
| B. | 锌粒与稀醋酸反应:Zn+2H+═Zn2++H2↑ | |
| C. | 浓盐酸与MnO2反应制Cl2:MnO2+2H++2Cl-═Mn2++Cl2↑+2H2O | |
| D. | 向含I-的酸性溶液中加入H2O2:H2O2+2H++2I-═I2+2H2O |
14.下列有机物不能通过加成反应制取的是( )
| A. | CH3-CH2OH | B. | CH3-COOH | C. | CH2Cl-CH2Cl | D. | CH3CH2Cl |
1.某同学组装了如图所示的电化学装置,则下列说法正确的是( )
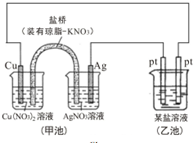

| A. | 实验过程中,甲池左侧烧杯中NO3-的浓度增大 | |
| B. | 图中甲池中的盐桥可以是装琼脂的饱和KCl溶液 | |
| C. | 若乙池为Na2SO4溶液,一段时间后,右边Pt极上产生了0.672L气体(标准状况),则甲池中Ag电极质量增加12.96g | |
| D. | Cu电极发生还原反应 |
18.下列实验方案中,能达到实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 比较苯酚和乙醇中羟基氢的活泼性强弱 | 用氢氧化钠分别与苯酚和乙醇反应 |
| B | 证明HOCH2CH2CHO中含有醛基 | 滴入KMnO4酸性溶液 |
| C | 检验Fe(NO3)2晶体是否已氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变成红色 |
| D | 检验乙醇与浓硫酸共热是否产生乙烯 | 将乙醇与浓硫酸共热至170℃,所得气体通入酸性高锰酸钾溶液中,观察溶液是否褪色 |
| A. | A | B. | B | C. | C | D. | D |
15.X、Y、Z均为短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z-,Y+和Z-具有相同的电子层结构.下列说法正确的是( )
| A. | 原子最外层电子数:X>Y>Z | B. | 原子序数:X>Y>Z | ||
| C. | 单质沸点:Z>Y>X | D. | 离子半径:X2->Y+>Z- |
 .
. .
.