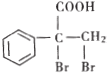
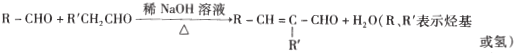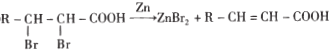��Ŀ����
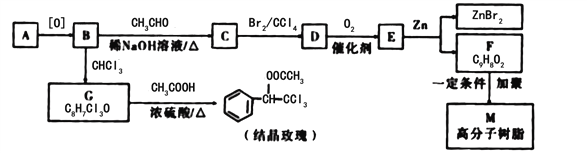
����Ŀ��������һ����Ҫ�Ļ���ԭ�ϣ���ҵ�ϲ��ð��Ĵ��������Ʊ����ᡣ
(1) ��֪��ӦN2(g)+3H2(g) 2NH3(g)Ϊ���ȷ�Ӧ���ں�����������˵���÷�Ӧ�ﵽƽ��״̬������_______��
A.������N2��H2��NH3��Ũ��֮��Ϊ1:2:3
B. v��(N2)=v��(H2)
C.������ѹǿ���ֲ���
D.���������ܶȱ��ֲ���
(2)������,Ϊ������ƽ��ʱ��ת����,�ɲ�ȡ�Ĵ�ʩ��_____________(Ҫ��������)
�Ǻϳɰ������Ĵ����������˹��̵�����Ҫ;��,�ϳɰ���Ӧ��ƽ�ⳣ��Kֵ���¶ȵĹ�ϵ���±�����400��ʱ,���ijʱ�̵��������������������ʵ���Ũ�ȷֱ�Ϊ1 mol��L-1��2 mol��L-1��3 mol��L-1ʱ,��ʱ�̸÷�Ӧ����Ӧ����_____ �淴Ӧ����(����ڡ�����С�ڡ����ڡ���
�¶�/�� | 200 | 300 | 400 |
K | 1.0 | 0.86 | 0.5 |
(4)�������Ṥ��β����һ�ַ������ü������ԭ���������֪��
�� CH4 (g)��2O2(g)��CO2(g)��2H2O(g) �� H����890.3 kJ��mol-1
�� N2(g)��2O2(g)��2NO2(g) �� H����67.0 kJ��mol-1
��CH4(g)��NO2(g)��ԭΪN2(g)�ȵ��Ȼ�ѧ����ʽΪ___________________________________________
(5)��25 ���£���Ũ�Ⱦ�Ϊ0.1 mol��L-1��MgCl2��CuCl2�����Һ����μ��백ˮ��������____����(�ѧʽ)�������ֳ�������ʱ,��Һ��C(Mg2+)/C(Cu2+)=_________(��֪25 ��ʱKsp[Mg(OH)2]=1.8��10-11��Ksp[Cu(OH)2]=2.2��10-20)
���𰸡� C ���¡���ѹ�����백�� С�� CH4(g)+2NO2(g) 2N2 (g) +CO2(g)+ 2H2O(g) ��H=-823.3kJ/mol Cu(OH)2 8.2��108 ��9��109 / 11
����������1�����淴Ӧ�ﵽƽ��ʱ, v��=v�� (ͬ�����ʱ�ʾ)����������֮�ȵ��ڻ�ѧ������֮��(��ͬ���ʱ�ʾ),��Ӧ��������ֵ����ʵ�����Ũ�ȡ��������ٱ仯,�Լ��ɴ�������һЩ��Ҳ�������仯,�ɴ˽����ж�����2�����ݷ�Ӧ�ص��������ƽ��ת���ʵĴ�ʩ����3������Ũ���̺�ƽ�ⳣ����Դ�С�ж�ƽ���ƶ����Ӷ��ƶ����淴Ӧ���ʴ�С����4�����ݸ�˹���ɼ��㷴Ӧ�ȣ���д�Ȼ�ѧ����ʽ����5�������ܶȻ����㡣
���: ��1��A. ������N2��H2��NH3��Ũ��֮��Ϊ1:2:3������˵����Ӧ��������ֵ�Ũ�Ȳ��ٱ仯,����Aѡ���Ǵ������B.���ﵽƽ��״̬ʱ, 3v��(N2)=v��(H2),��B������
C.��Ӧǰ�������������ͬ��ѹǿ����˵����Ӧ�ﵽƽ��״̬,��C��ȷ��D.������������������,�����ݻ�Ϊ��ֵ,�����ܶ���ʼ���ղ���,����˵���ﵽƽ��,��D����������Cѡ������ȷ����
��2�����ڸ÷�ӦΪ���������С�ķ��ȷ�Ӧ������ͨ�����¡���ѹ�����백���ȴ�ʩ����ƽ��ʱ��ת���ʣ���˱����Ϊ�����¡���ѹ�����백����
(3)QC=![]() =2.25>K=0.5��˵����Ӧ���淴Ӧ������������v��(N2)=v��(N2)����ˣ�������ȷ����: С�ڣ�
=2.25>K=0.5��˵����Ӧ���淴Ӧ������������v��(N2)=v��(N2)����ˣ�������ȷ����: С�ڣ�
��4���� CH4 (g)��2O2(g)��CO2(g)��2H2O(g) �� H����890.3 kJ��mol-1
�� N2(g)��2O2(g)��2NO2(g) �� H����67.0 kJ��mol-1
���ݸ�˹��������-�ڵã�CH4(g)+2NO2(g) 2N2 (g) +CO2(g)+ 2H2O(g) ��H=-823.3kJ/mol��
��ˣ�������ȷ����: CH4(g)+2NO2(g) 2N2 (g)+CO2(g)+ 2H2O(g) ��H=-823.3kJ/mol��
��5������Ksp[Cu(OH)2]<Ksp[Mg(OH)2]������������Cu(OH)2�����������ֳ�������ʱ����Һ��Cu(OH)2��Mg(OH)2�ı�����Һ����Һ��OH-����Ũ����ͬ�������ܶȻ��������㣬��Һ��C(Mg2+)/C(Cu2+)=![]() =
=![]() =8.2��108��
=8.2��108��
�ʴ�Ϊ��8.2��108 ��9��109 / 11��