题目内容
【题目】下列有关说法正确的是( )
A. 吸热反应一定不可以自发进行
B. 在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的方向
C. NH4HCO3(s)=NH3(g)+H2O(g)+CO2(g) △H=+185.57KJ/mol,能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向
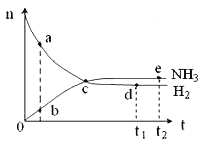
D. N2(g)+3H2(g)![]() 2NH3(g)△H<0,其他条件不变时升高温度,反应速率V(H2),平衡逆移,氢气的平衡转化率均减小
2NH3(g)△H<0,其他条件不变时升高温度,反应速率V(H2),平衡逆移,氢气的平衡转化率均减小
【答案】C
【解析】
A、反应能自发进行是根据熵判据和焓判据的复合判据来判断的,不能单独根据焓变判断,故A错误;B、在其他条件不变的情况下,催化剂只改变反应速率,不改变平衡移动,所以不可以改变化学反应进行的方向,故B错误;C、该反应为吸热反应,不能自发进行;而最终该反应能自发进行,则主要原因是体系有自发地向混乱度增加的方向转变的倾向,故C正确;D、升高温度,反应速率V(H2)增大,平衡逆向移动,氢气转化率减小,故D错误;故选C。

【题目】煤的气化主要反应是煤中碳与水蒸气反应生成CO、H2等。回答下列问题:
(1)CO与H2分别与O2都可以设计成燃料电池。CO与O2设计成燃料电池(以熔融碳酸盐为电解质)负极的电极反应为:______________;
(2)在煤的气化获得的化工原料气中含有少量羰基硫(COS),能引起催化剂中毒、大气污染等。COS的电子式为___________;羰基硫与烧碱溶液反应生成水喝两种正盐的离子方程式为:__________;羰基硫的脱硫常用两种方法,其反应式分别为:
①氢解反应:COS(g) + H2(g) = H2S(g) + CO(g) ΔH1 =+7kJ/mol
②水解反应:COS(g) + H2O(g) = H2S(g) + CO2(g) ΔH2
已知反应中相关的化学键键能数据如下:
化学键 | C=O(CO2) | C=O(COS) | C=S | H-S | H-O |
键能(kJ/mol) | 803 | 742 | 577 | 339 | 465 |
则ΔH2 =____________kJ/mol。
(3)脱硫处理后的CO和H2在催化剂作用下合成甲醇:
CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH2 =-90.14kJ/mol。该反应能自发的理由是_______
CH3OH(g)+H2O(g) ΔH2 =-90.14kJ/mol。该反应能自发的理由是_______
①一定温度下,在两个容积都为为VL的恒容莫比容器中,按如下方式加入反应物,一段时间后达到平衡:
容器 | 甲 | 乙 |
反应物投入量 | 1molCO2、3molH2 | a molCO2、3a molH2、 n molCH3OH(g)、n molH2O(g) |
若甲中平衡后气体的压强为开始的0.8倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则n的取值范围为_____________;
②甲容器保持恒容,欲增大H2的平衡转化率,可采取的措施有:________(答两点即可)