��Ŀ����
����Ŀ���״�����Ҫ�Ļ�ѧ��ҵ����ԭ�Ϻ����Һ��ȼ�ϣ���ҵ�Ͽ�����CO��CO2������ȼ�ϼ״�����֪�״��Ʊ����йػ�ѧ��Ӧ�Լ��ڲ�ͬ�¶��µĻ�ѧ��Ӧƽ�ⳣ�������ʾ��
��ѧ��Ӧ | ƽ�� | �¶�/�� | |
500 | 800 | ||
��2H2��g��+CO��g��CH3OH��g�� | K1 | 2.5 | 0.15 |
��H2��g��+CO2��g��H2O��g��+CO��g�� | K2 | 1.0 | 2.50 |
��3H2��g��+CO2��g��CH3OH��g��+H2O��g�� | K3 | ||
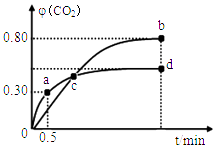
��1���ݷ�Ӧ����ڿ��Ƶ���K1��K2��K3֮��Ĺ�ϵ����K3=����K1��K2��ʾ����500��ʱ��÷�Ӧ����ijʱ�̣�H2��g����CO2��g����CH3OH��g����H2O��g����Ũ�ȣ�molL��1���ֱ�Ϊ0.8��0.1��0.3��0.15�����ʱv��v�������������=����������
��2�����ڷ�Ӧ�ۣ�����ͬ�¶Ⱥ��ݻ�����ʱ����˵���÷�Ӧ�Ѵ�ƽ��״̬����
A.n��CO2����n��H2����n��CH3OH����n��H2O��=1��3��1��1
B.������ѹǿ���ֲ���
C.H2������������CH3OH����������֮��Ϊ3��1
D.�����ڵ��ܶȱ��ֲ��䣮
���𰸡�
��1��K1?K2,��
��2��B,C
���������⣺��1����Ӧ��3H2��g��+CO2��g���TCH3OH��g��+H2O��g�������������С�ķ�Ӧ��S��0�����ݷ�Ӧ��+�ڵõ���Ӧ�ۣ�����ƽ�ⳣ��K3=K1��K2������¶ȱ仯���������¶����ߣ�ƽ�ⳣ����С��ƽ��������У������жϷ�Ӧ�Ƿ��ȷ�Ӧ���ʱ��H��0����500�桢2L���ܱ������У����з�Ӧ�ۣ���÷�Ӧ����ijʱ�̣�H2��g����CO2��g����CH3OH��g����H2O ��g����Ũ�ȣ�mol/L���ֱ�Ϊ0.8��0.1��0.3��0.15��Q= ![]() =0.87��K=2.5����Ӧ������У�V����V�棬
=0.87��K=2.5����Ӧ������У�V����V�棬
��2��A��n��CO2����n��H2����n��CH3OH����n��H2O��=1��3��1��1�������ж����淴Ӧ�����Ƿ���ȣ����ж��Ƿ�ﵽƽ��״̬����A����
B���÷�Ӧ�������С�ķ�Ӧ��������ѹǿ���ֲ��䣬�������淴Ӧ������ȣ�����ֵ�Ũ�Ȳ��ٱ仯���ﵽ��ƽ��״̬����B��ȷ��
C��H2������������CH3OH����������֮��Ϊ3��1����ʾ�������淴Ӧ���ʣ��������������ϵ��˵���ﵽ��ƽ��״̬����C��ȷ��
D�������ڵ��ܶȱ��ֲ��䣬��Ӧ����ʽ���߶������壬��������������䣬�������ݻ��̶������Է�Ӧ������������ܶ�ʼ�ղ��䣬�����ܶȲ�����Ϊ�ж�ƽ��״̬�����ݣ���D����
���Դ��ǣ���1��K1K2��������2��BC
�����㾫�������ڱ��⿼��Ļ�ѧƽ��״̬���жϺͻ�ѧƽ��ļ��㣬��Ҫ�˽�״̬�жϣ���v(B��)=v(B��)��v(C��):v(D��)=x : y��c(C)��C%��n(C)%�Ȳ������A��B��C��DΪ���壬��m+n��x+y��ѹǿ�㶨����ϵ��ɫ�����λʱ����ij�����ڻ�ѧ���Ķ����������γ�������ϵƽ��ʽ���㶨��m+n �� x+y���ȣ���Ӧ��ת����=ת��Ũ�ȡ���ʼŨ�ȡ�100%=ת�����ʵ�������ʼ���ʵ�����100%����Ʒ�IJ���=ʵ�����ɲ�������ʵ����������Ͽɵõ���������ʵ�����100%���ܵó���ȷ�𰸣�

 ѧ���쳵�����ּ��ں�����ҵϵ�д�
ѧ���쳵�����ּ��ں�����ҵϵ�д� ��˼ά������ҵϵ�д�
��˼ά������ҵϵ�д�