题目内容
【题目】分某实验室需要配制480mL0.10mol/LNa2CO3溶液。
(1)实验时,应用托盘天平称取十水和碳酸钠晶体________g。
(2)所需玻璃仪器有:玻璃棒、烧杯、100mL量筒、__________、________。
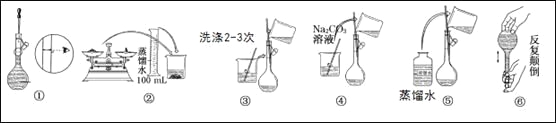
(3)实验时图中所示操作的先后顺序为________ (填编号)。
(4)在配制过程中,下列操作对所配溶液浓度有无影响?__________(填“偏高”、“偏低”或“无影响”)
①称量时误用“左码右物”
②转移溶液后没有洗涤烧杯和玻璃棒
③向容量瓶加水定容时俯视液面
④摇匀后液面下降,再加水至刻度线
(5)若改用浓溶液稀释,需要量取2mol/LNa2CO3溶液____________mL。
【答案】(1)14.3;
(2)500mL容量瓶;胶头滴管;
(3)②④③⑤①⑥;
(4)偏低;偏低;偏高;偏低;(5)25;
【解析】试题分析:(1)因配制溶液的体积为480ml,而容量瓶的规格没有480ml,只能选用500ml,Na2CO3的物质的量n=cV=0.5L×0.1molL-1=0.05mol,Na2CO310H2O的物质的量等于Na2CO3的物质的量,所以Na2CO310H2O的质量0.05mol×286g/mol=14.3g,故答案为:14.3;
(2)根据配制过程,所以需要的仪器为:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管,故答案为:500mL容量瓶;胶头滴管;
(3)配制顺序是:计算→称量→溶解、冷却→移液→洗涤→定容→摇匀→装瓶贴签,故答案为:②④③⑤①⑥;
(4)①称量时误用“左码右物”,导致溶质的物质的量偏小,浓度偏低,故答案为:偏低;
②转移溶液后没有洗涤烧杯和玻璃棒,导致溶质的物质的量偏小,浓度偏低,故答案为:偏低;
③向容量瓶加水定容时俯视液面,导致溶液的体积偏小,浓度偏高,故答案为:偏高;
④摇匀后液面下降,再加水至刻度线,导致溶质的物质的量偏小,浓度偏低,故答案为:偏低;
(5)稀释前后,溶质的物质的量,设需要量取2mol/LNa2CO3溶液为V,则2mol/L×V=0.1mol/L×500ml,解得V=0.025L=25mL,故答案为:25。

 全能练考卷系列答案
全能练考卷系列答案【题目】已知硫代硫酸钠溶液与稀H2SO4反应可析出单质硫沉淀:Na2S2O3+H2SO4===Na2SO4+S↓+SO2↑+H2O,某同学按下表进行实验,请你判断哪一组先出现浑浊。
编号 | 加3%Na2S2O3/mL | 加1∶5的H2SO4/滴 | 温度/℃ |
1 | 5 | 25 | 25 |
2 | 5 | 15 | 35 |
3 | 5 | 25 | 45 |