题目内容
6.下列离子水解的离子方程式中正确的是( )| A. | HCO3-+H2O?CO2↑+H2O+OH- | B. | HS-+H2O?H3O++S2- | ||
| C. | Fe3++3H2O?Fe(OH)3↓+3H+ | D. | CO32-+H2O?HCO3-+OH- |
分析 A.碳酸氢根离子水解生成碳酸和氢氧根离子;
B.水解生成氢硫酸和氢氧根离子;
C.水解程度很弱,不能生成沉淀;
D.碳酸根离子水解生成碳酸氢根离子和氢氧根离子.
解答 解:A.水解离子反应为HCO3-+H2O?H2CO3+OH-,故A错误;
B.HS-+H2O?H3O++S2-为电离方程式,水解离子反应为HS-+H2O?H2S+OH-,故B错误;
C.水解离子反应为Fe3++3H2O?Fe(OH)3+3H+,故C错误;
D.水解离子反应为CO32-+H2O?HCO3-+OH-,故D正确;
故选D.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握盐类水解原理及离子反应的书写方法为解答的关键,侧重水解离子反应的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.钢铁“发蓝”是将钢铁制品浸到某些氧化性的溶液中,在钢铁的表面形成一层四氧化三铁的技术过程.其中一种办法是将钢铁制品浸到亚硝酸钠和浓氢氧化钠的混合溶液中加热到130℃反应.其过程可以用如下化学方程式表示:
①3Fe+NaNO2+5NaOH=3Na2FeO2+H2O+NH3↑;
②Na2FeO2+NaNO2+H2O═Na2Fe2O4+NH3↑+NaOH (未配平);
③Na2FeO2+Na2Fe2O4+2H2O=Fe3O4+4NaOH;
下列说法不正确的是( )
①3Fe+NaNO2+5NaOH=3Na2FeO2+H2O+NH3↑;
②Na2FeO2+NaNO2+H2O═Na2Fe2O4+NH3↑+NaOH (未配平);
③Na2FeO2+Na2Fe2O4+2H2O=Fe3O4+4NaOH;
下列说法不正确的是( )
| A. | 碱性条件下,NaNO2的氧化性比Na2FeO2、Na2Fe2O4都强 | |
| B. | 反应 ①、②、③均是氧化还原反应 | |
| C. | 反应 ②配平后,H2O的化学计量数是5 | |
| D. | 整个反应过程中每有16.8g Fe参加反应转移0.8mol电子 |
11.关于FeCl3溶液水解的错误说法是( )
| A. | FeCl3水解使溶液呈酸性,并能起净水作用,使水中悬浮的杂质沉降 | |
| B. | 浓度为5mol•L-1和0.5mol•L-1的两种FeCl3溶液,其它条件相同时,Fe3+离子的水解程度前者比后者低 | |
| C. | 加热FeCl3溶液并蒸干,再灼烧,此时得到的固体是无水氯化铁 | |
| D. | 为了抑制Fe3+的水解,更好地保存FeCl3溶液,应向其中加入少量的盐酸 |
13.在一定温度下的恒容密闭容器中,取一定量的A、B于反应容器中,当下列物理量(或比值)不再改变时,不能表明反应A(s)+2B(g)?C(g)+D(g) 已达平衡状态的是( )
| A. | 混合气体的密度 | B. | 气体B、C的物质的量浓度之比 | ||
| C. | 气体B、D的质量之比 | D. | 气体C、D的物质的量之比 |

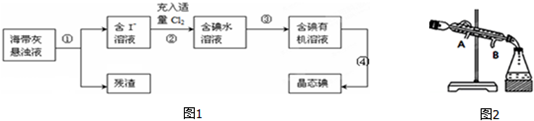
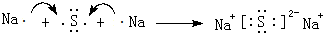 .
.