题目内容
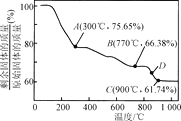
【题目】MnCO3在空气中加热易转化为不同价态的锰的氧化物,其固体残留率随温度的变化如图所示(其中A、B、C点对应的物质均为纯净物,D点对应的物质为混合物)。下列说法正确的是
A.A点对应物质为MnO
B.B点对应物质为Mn3O4
C.C点对应物质为MnO2
D.D点对应物质为Mn2O3和MnO的混合物
【答案】B
【解析】
A. 设MnCO3的物质的量为1mol,即质量为115g,A点剩余固体质量为115g×75.65%=87g,减少的质量为115g87g=28g,可知MnCO3失去的组成为CO,故剩余固体的成分为MnO2,A项错误;
B. B点剩余固体质量为115g×66.38%=76.337g,根据锰元素守恒知m(Mn)=55g,则m(O)=76.337g55g=21.337g,则n(Mn):n(O)=![]() :
:![]() =3:4,故剩余固体的成分为Mn3O4,B项正确;
=3:4,故剩余固体的成分为Mn3O4,B项正确;
C. C点剩余固体质量为115g×61.74%=71g,根据锰元素守恒知m(Mn)=55g,则m(O)=71g55g=16g,则n(Mn):n(O)=![]() =1:1,故剩余固体的成分为MnO,C项错误;
=1:1,故剩余固体的成分为MnO,C项错误;
D. 因D点介于B、C点之间,故D点对应固体的成分为Mn3O4与MnO的混合物,D项错误;
答案选B。

【题目】在相同条件下,做H2O2分解对比实验时,回答下面问题:
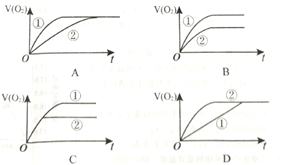
(1)其中①加人MnO2催化,②不加MnO2催化。下图是反应放出O2的体积随时间的变化关系示意图,其中正确的是_______________
(2)将质量相同但聚集状态不同的MnO2分别加入到5 mL 5%的双氧水中,并用带火星的木条测试。测定结果如下:
催化剂(MnO2) | 操作情况 | 观察结果 | 反应完成所需的时间 |
粉末状 | 混合不振荡 | 剧烈反应,带火星的木条复燃 | 3.5分钟 |
块状 | 反应较慢,火星红亮但木条不复燃 | 30分钟 |
①写出H2O2的电子式______________发生的化学反应方程式_______________________。
②实验结果说明催化剂作用的大小与____________有关。
【题目】某小组同学为探究H2O2、H2SO3、Br2的氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。
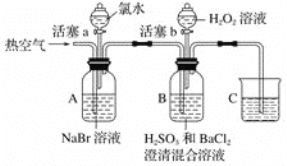
实验记录如下:
实验操作 | 实验现象 | |
Ⅰ | 打开活塞a,滴加氯水,关闭活塞a | A中溶液变为红棕色 |
Ⅱ | 吹入热空气 | A中红棕色明显变浅;B中有气泡,产生大量白色沉淀,混合液颜色无明显变化 |
Ⅲ | 停止吹入空气,打开活塞b,逐滴加入H2O2溶液 | 开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色 |
请回答下列问题:
(1)A中反应的离子方程式是______。
(2)实验操作Ⅱ吹入热空气的目的是_____。
(3)装置C的作用是_____,C中盛放的药品是_____。
(4)实验操作Ⅲ,混合液逐渐变成红棕色,其对应的离子方程式是_____。
(5)由上述实验得出的结论是______。
(6)实验反思:
①有同学认为实验操作Ⅱ吹入的热空气,会干扰(5)中结论的得出,你认为是否干扰,理由是________。
②实验操作Ⅲ,开始时颜色无明显变化的原因是(写出一条即可)______。