题目内容
x、y为短周期元素,x原子K、L、M各电子层的电子数之比为1:4:1,它比y原子多3个电子,下列叙述正确的是( )
| A.x离子半径大于y离子半径 |
| B.x单质在空气中燃烧可生成两种化合物 |
| C.x、y形成的化合物与浓硫酸共热可在烧瓶中进行 |
| D.电解x、y形成的化合物的水溶液可得到y单质 |
B
分析:由X原子各电子层的电子数比为1:4:1,可知X原子核外有3个电子层,由电子排布规律可知,K层最多不超过2个电子且排满后才能排L层,所以得到X为Mg,从而可知Y是F元素,根据Mg和F元素对应单质及化合物的性质解答该题.
解:由X原子各电子层的电子数比为1:4:1,可知X原子核外有3个电子层,由电子排布规律可知,K层最多不超过2个电子且排满后才能排L层,所以得到X为Mg,从而可知Y是F元素.
A、对电子层结构相同的离子,核电荷数越大,离子半径就越小,故A错误;
B、Mg在空气中燃烧时既与O2反应生成MgO,也与N2反应生成Mg3N2,故B正确;
C、MgF2与浓H2SO4共热时会生成HF,对玻璃会有强烈的腐蚀作用,所以不能在烧瓶中进行实验,故C错误;
D、在水溶液中不可能得到F2,因为F2与水剧烈反应生成HF和O2,故D错误;
故选B.

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目
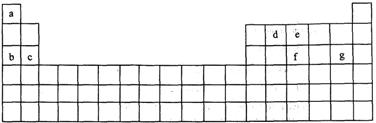
 数的2倍。
数的2倍。 试回答:
试回答: W_________。
W_________。