题目内容
几种短周期元素的原子半径及主要化合价如下表:
下列叙述正确的是
A.化合物WV2常用于食品的漂白
B.X离子和W离子具有相同的电子层结构
C.单质与等浓度的稀盐酸反应的剧烈程度:X>Y
D.X和Y的最高价氧化物对应的水化物都能溶于NaOH溶液
| 元素代号 | X | Y | Z | W | V |
| 原子半径/pm | 160 | 143 | 89 | 104 | 66 |
| 主要化合价 | +2 | +3 | +2 | +6、+4、– 2 | –2 |
A.化合物WV2常用于食品的漂白
B.X离子和W离子具有相同的电子层结构
C.单质与等浓度的稀盐酸反应的剧烈程度:X>Y
D.X和Y的最高价氧化物对应的水化物都能溶于NaOH溶液
C
短周期元素中,W的主要化合价有+6、+4、– 2的为S元素;V的主要化合价– 2的为O元素;对比X、Z的原子半径得X为Mg元素、Z为Be元素;Y为AL元素;
A错,化合物WV2是SO2,不能用于漂白食品,会有致癌物质生成;B错,X离子为AL3+W离子为S2—,电子结构不同;C正确,镁的金属性比铝强,与盐酸反应更剧烈;D错,氢氧化铝是典型的两性氢氧化物,与氢氧化钠能反应,但氢氧化镁不能与氢氧化钠反应;
A错,化合物WV2是SO2,不能用于漂白食品,会有致癌物质生成;B错,X离子为AL3+W离子为S2—,电子结构不同;C正确,镁的金属性比铝强,与盐酸反应更剧烈;D错,氢氧化铝是典型的两性氢氧化物,与氢氧化钠能反应,但氢氧化镁不能与氢氧化钠反应;

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案
相关题目
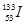 。下列有关叙述正确的是 ( )
。下列有关叙述正确的是 ( )