题目内容
10.下列物质中,在常温常压时呈气态的是( )| A. | 乙醇 | B. | 苯 | C. | 甲醛 | D. | 四氯化碳 |
分析 A、乙醇常温下是液体;
B、常温下,苯为液态;
C、常温下,甲醛为气体;
D、常温下,四氯化碳是液体.
解答 解:A、常温下,乙醇是液体不是气体,故A错误;
B、由于苯常温下是液体,不是气态,故B错误;
C、常温下,甲醛为一种刺激性气味的气体,故C正确;
D、四氯化碳常温下是液体不是气体,故D错误;
故选C.
点评 本题考查了常见有机物在常温下的状态,需要记住一些常见有机物的状态,本题难度不大.

练习册系列答案
相关题目
20.常温下,某无色溶液能与铝反应放出氢气,该溶液中一定能大量存在的离子组是( )
| A. | Na+、K+、MnO4-、SO42- | B. | Mg2+、NH4+、SO42-、Cl- | ||
| C. | Na+、Cl-、K+、SO42- | D. | Na+、K+、CO32-、NO3- |
1.下列关于金属钠性质的叙述中,正确的是( )
| A. | 钠是密度小、硬度大、熔点高的银白色金属 | |
| B. | 钠在纯净的氧气中充分燃烧,生成白色固体Na2O | |
| C. | 将金属钠放入CuSO4溶液中,可观察到大量红色的铜析出 | |
| D. | 将金属钠放入水中立即熔化成小球,说明金属钠熔点低,且反应放出热量 |
5.某有机物甲经氧化后得到乙(C2H3O2Cl),而甲经水解可得到丙.1mol丙和2mol乙反应可得到一种含氯的酯(C6H8O4Cl2).以此推断甲的结构简式为( )
| A. |  | B. |  | C. |  | D. | HO-CH2-CH2OH |
15.在一密闭容器中充入一种气态烃和足量的氧气,用电火花点燃完全燃烧后,容器内气体体积保持不变,若气体体积均在120℃和相同的压强下测定的,这种气态烃可能是( )
| A. | C2H2 | B. | C2H4 | C. | C2H6 | D. | C3H6 |
2.寻找清洁能源一直是化学家努力的方向,下列关于能源的说法错误的是( )
| A. | 氢气热值高,其燃烧产物是水,是一种理想的清洁燃料 | |
| B. | 利用太阳能等清洁能源代替化石燃料,有利于节约资源,保护环境 | |
| C. | 煤的气化技术在一定程度上实现了煤的高效、清洁利用 | |
| D. | 石油作为重要的可再生能源应该被尽量地利用 |
9.欲降低废水中重金属元素铬的毒性,可将Cr2O72-转化为Cr(OH)3沉淀除去.三种金属离子生成沉淀的pH如右表.
某含铬废水处理的主要流程如图所示:
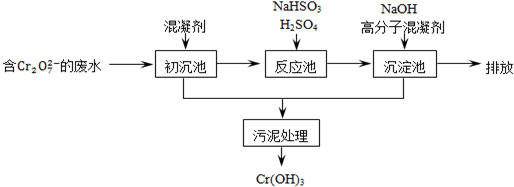
(1)Cr在周期表中的位置为第四周期第ⅥB族.
(2)初沉池中加入明矾作沉降剂,其作用的原理是(用离子方程式表示)
Al3++3H2O?Al(OH)3+3H+.
(3)请补充并配平以下反应池中发生主要反应的离子方程式:
1Cr2O72-+3HSO3-+5H+=2Cr3++3SO42-+4H2O.
(4)根据“沉淀法”和“中和法”的原理,向沉淀池中加入NaOH溶液,此过程中发生主要反应的离子方程式是:H++OH-=H2O和Cr3++3OH-=Cr(OH)3↓.证明Cr3+沉淀完全的方法是取沉淀后的上层清液测定其pH,若pH≥8,则沉淀完全.
| 开始沉淀的pH | 完全沉淀的pH | |
| Fe(OH)2 | 7.0 | 9.0 |
| Fe(OH)3 | 1.9 | 3.2 |
| Cr(OH)3 | 6.0 | 8.0 |

(1)Cr在周期表中的位置为第四周期第ⅥB族.
(2)初沉池中加入明矾作沉降剂,其作用的原理是(用离子方程式表示)
Al3++3H2O?Al(OH)3+3H+.
(3)请补充并配平以下反应池中发生主要反应的离子方程式:
1Cr2O72-+3HSO3-+5H+=2Cr3++3SO42-+4H2O.
(4)根据“沉淀法”和“中和法”的原理,向沉淀池中加入NaOH溶液,此过程中发生主要反应的离子方程式是:H++OH-=H2O和Cr3++3OH-=Cr(OH)3↓.证明Cr3+沉淀完全的方法是取沉淀后的上层清液测定其pH,若pH≥8,则沉淀完全.
 ;
;