题目内容
【题目】某校化学兴趣小组根据反应:H2O2+2HI=2H2O+I2探究影响化学反应速率的因素。实验数据如下:
实验 编号 | H2O2溶液浓度/(mol·L-1) | HI溶液浓度/(mol·L-1) | 温度/℃ | 反应速率/(mol·L-1·s-1) |
① | 0.1 | 0.1 | 25 | 0.0076 |
② | 0.1 | 0.2 | 25 | 0.0153 |
③ | 0.1 | 0.3 | 25 | 0.0227 |
④ | 0.1 | 0.1 | 35 | 0.0304 |
回答下列问题:
(1)反应:H2O2+2HI=2H2O+I2中,氧化剂是___。
(2)25℃时,表明增大反应物浓度,化学反应速率___(填“增大”或“减小”)。
(3)能表明温度对化学反应速率影响的实验编号是①和___。
(4)H2O2不稳定,写出H2O2发生分解反应的化学方程式:___。
【答案】H2O2 增大 ④ 2H2O2![]() 2H2O+O2↑
2H2O+O2↑
【解析】
(1)反应:H2O2+2HI=2H2O+I2中氧元素化合价降低,得到电子,氧化剂是H2O2。
(2)根据表中数据可知25 ℃时,增大反应物浓度,化学反应速率增大。
(3)要探究温度对反应速率的影响,其他条件不变,因此根据表中数据可知能表明温度对化学反应速率影响的实验编号是①和④。
(4)H2O2不稳定,易分解生成氧气和水,则H2O2发生分解反应的化学方程式为2H2O2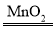 2H2O+O2↑。
2H2O+O2↑。

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目