题目内容
下列各组物质,化学键类型相同、晶体类型相同且熔化时破坏作用力类型也相同的 ( )
| A.HCl KCl | B.CO2 SiO2 | C.NH4Cl CCl4 | D.NaOH Na2O2 |
D
解析试题分析:A、HCl含有共价键,是分子晶体,熔化时破坏分子间作用力,KCl含有离子键,是离子晶体,熔化时破坏离子键,均不同,错误;B、CO2含有共价键,是分子晶体,熔化时破坏分子间作用力,SiO2含有共价键,是原子晶体,熔化时破坏共价键,错误;C、NH4Cl含有离子键,是离子晶体,熔化时破坏离子键, CCl4含有共价键,是分子晶体,熔化时破坏分子间作用力,错误;D、NaOH、 Na2O2都含有离子键,是离子晶体,熔化时都破坏离子键,完全相同,正确,答案选D。
考点:考查对化学键、晶体类型、熔化时破坏的作用力的判断

练习册系列答案
相关题目
关于含正离子N5+的化合物N5ASF6,下列叙述中错误的是( )
| A.N5+共有34个核外电子 | B.N5+中氮原子间以共价键结合 |
| C.化合物N5ASF6中AS的化合价为+1价 | D.化合物N5ASF6中F的化合价为 -1价 |
下列过程中,共价键被破坏的是
| A.碘升华 | B.溴蒸气被木炭吸附 | C.蔗糖溶于水 | D.氯化氢气体溶于水 |
下列分子或离子中,不存在sp3杂化类型的是
| A.SO42- | B.NH3 | C.C2H6 | D.SO2 |
下列对一些实验事实的理论解释正确的是
| 选项 | 实验事实 | 理论解释 |
| A | 氮原子的第一电离能大于氧原子 | 氮原子2p能级半充满 |
| B | CO2为直线形分子 | CO2分子中C—O是极性键 |
| C | 金刚石的熔点低于石墨 | 金刚石是分子晶体,石墨是原子晶体 |
| D | HF的沸点高于HCl | HF的相对分子质量小于HCl |
观察下列模型并结合有关信息,判断有关说法正确的是
| | 硼晶体的结构单元 | SF6分子 | S8分子 | NaCl |
| 结构模型示意图 | 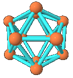 | 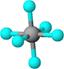 | 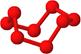 | 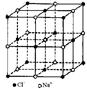 |
| 备注 | 熔点1873K | / | 易溶于CS2 | / |
A.单质硼属分子晶体,其结构单元B12中含有30个B-B键,含20个正三角形
B.SF6是由极性键构成的分子
C.固态硫S8属于原子晶体
D.NaCl熔化和溶于水均能产生自由移动的离子,且破坏的是同种作用力,NaCl晶胞中每个Na+周围最近且等距离的Na+有6个
氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为 ( )
| A.两种分子的中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化。 |
| B.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强。 |
| C.NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道。 |
| D.氨气分子是极性分子而甲烷是非极性分子。 |
已知:
下列说法不正确的是
| A.①和②变化过程中都会放出热量 |
| B.氯原子吸引电子的能力强于钠原子和氢原子 |
| C.①和②中的氯原子均得到1个电子达到8电子稳定结构 |
| D.NaCl中含有离子键,HCl中含有共价键 |
SF6是一种无色气体,具有很强的稳定性,可用于灭火。SF6的分子结构如下图所示,呈正八面体型。如果F元素有两种稳定的同位素,则SF6的不同分子种数为 ( )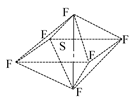
| A.6种 | B.7种 | C.10种 | D.12种 |