��Ŀ����
����Ŀ��ijͬѧ������������ȡ��������(��Ҫ�ɷ�ΪFe2O3��SiO2��Al2O3����������������)��ȡ��ˮ����������(FeSO4��7H2O)��������������̣�

����˵������ȷ���ǣ� ��
A. �ܽ�����ѡ���������ᣬ�Լ�Xѡ������
B. ����1��һ������SiO2������pH��Ϊ��ʹAl3+ת��ΪAl(OH)3���������2
C. ����Һ2�õ�FeSO4��7H2O��Ʒ�Ĺ����У������������ֹ�������ͷֽ�
D. ���ı䷽��������Һ1��ֱ�Ӽ�NaOH���������õ��ij����������ܽ⣬����Һ���ᾧ����Ҳ�ɵõ�FeSO4��7H2O
���𰸡�D
��������
A�����������ͼ���������Fe2O3��Al2O3��ת��Ϊ�����Σ���ȥSiO2��Ȼ�������ۻ�ԭFe3+�õ�����������A��ȷ��B������1ΪSiO2������FeSO4��Al2(SO4)3���õ��ǵ���pH�ķ�����ʹAl3+ת��ΪAl(OH)3�����Ӷ���FeSO4���룬B����ȷ��C��Fe2+���ױ������������ڵõ�FeSO4��7H2O��Ʒ�Ĺ����У�Ҫ��ֹ�䱻�����ͷֽ⣬C��ȷ��D������Һ1��ֱ�Ӽӹ�����NaOH�õ�����Fe(OH)2��������Fe(OH)2���ȶ��������ױ�����ΪFe(OH)3�������Ļ����������õIJ�Ʒ���������н϶������Fe2(SO4)3��D����ȷ����ѡD��

����Ŀ����ͼ������������̽��SO2�����ʡ�ʵ��ʱ��Na2SO3�����ϵμ���Ũ���ᣬ��������һ������������档
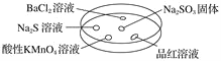
�±��ж�ʵ������������������Ľ��Ͳ���ȷ����(����)
ѡ�� | ʵ������ | ���� |
A | BaCl2��Һ����� | SO2��BaCl2��Һ��Ӧ������BaSO3���� |
B | Na2S��Һ����� | SO2��Na2S��Һ��Ӧ������S���� |
C | ����KMnO4��Һ��ɫ | SO2���л�ԭ�� |
D | Ʒ����Һ��ɫ | SO2����Ư���� |
A. A B. B C. C D. D