题目内容
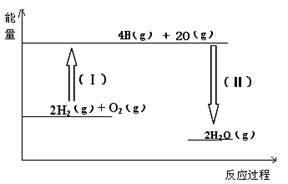
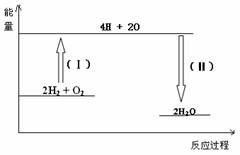
已知拆开1molH2需要消耗436kJ能量,拆开1molO2需要消耗496kJ能量,形成水分子中的1molH-O能够释放463kJ能量。根据以上所给的数据计算反应:
2H2(g)+O2(g)=2H2O(g) ;△H = 。
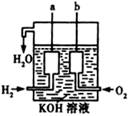
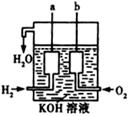
(2)如图所示,可形成氢氧燃料电池。通常氢氧燃料电池有酸式(当电解质溶液为H2SO4溶液时)和碱式[当电解质溶液为NaOH(aq)或KOH(aq)时]两种。试回答下列问题:
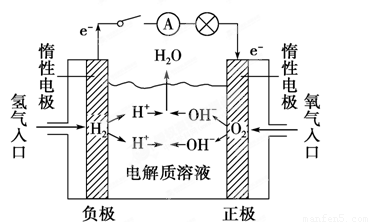
①酸式电池的电极反应:负极________________,正极______________;电池总反应:______________;电解质溶液pH的变化________(填“变大”、“变小”或“不变”)。
②碱式电池的电极反应:负极________________,正极______________;电池总反应:______________;电解质溶液pH的变化________(填“变大”、“变小”或“不变”)。
(1)-484kJ/mol
(2)①2H2-4e-=4H+ O2+4e-+4H+=2H2O 2H2+O2=2H2O 变大
②2H2-4e-+4OH-=4H2O O2+4e-+2H2O=4OH- 2H2+O2=2H2O 变小
【解析】
试题分析:(1)反应热就是断键吸收的能量和形成化学键所放出的能量的差值,则根据键能可知,该反应的反应热△H=436kJ/mol×2+496kJ/mol-2×2×463kJ/mol=-484kJ/mol。
(2)原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。因此在氢氧燃料电池中,氢气在负极通入,失去电子。氧气在正极通入,得到电子。
①如果是酸式电池,则电极反应是负极2H2-4e-=4H+,正极O2+4e-+4H+=2H2O;电池总反应:2H2+O2=2H2O;反应中有水生成,氢离子的浓度降低,所以电解质溶液pH变大。
①如果是碱式电池,则电极反应是负极2H2-4e-+4OH-=4H2O,正极O2+4e-+2H2O=4OH-;电池总反应:2H2+O2=2H2O;反应中有水生成,OH-的浓度降低,所以电解质溶液pH变小。
考点:考查反应热的计算、氢氧燃料电池中电极反应式的书写等
点评:该题是高考中的常见题型,属于中等难度的试题。试题在注重对学生基础知识巩固和训练的同时,侧重对学生灵活运用基础知识解决实际问题的能力的培养,有利于培养学生的灵活应变能力和规范答题能力。

 名校课堂系列答案
名校课堂系列答案 2C(g)+xD(g),经5min达到平衡,此时生成2 mol C,测得D的平均反应速率为0.15 mol/(L·min),则平衡时A的物质的量浓度是____________;B的转化率是__________;x的值是___________。
2C(g)+xD(g),经5min达到平衡,此时生成2 mol C,测得D的平均反应速率为0.15 mol/(L·min),则平衡时A的物质的量浓度是____________;B的转化率是__________;x的值是___________。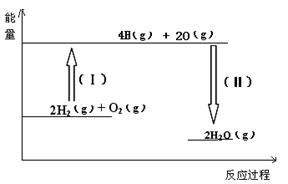
 2C(g)+xD(g),经5min达到平衡,此时生成2 mol C,测得D的平均反应速率为0.15 mol/(L·min),则平衡时A的物质的量浓度是____________;B的转化率是__________;x的值是___________。
2C(g)+xD(g),经5min达到平衡,此时生成2 mol C,测得D的平均反应速率为0.15 mol/(L·min),则平衡时A的物质的量浓度是____________;B的转化率是__________;x的值是___________。