题目内容
(本小题满分9分)
(1)把6
mol A气体和5 mol B气体混合放入4 L密闭容器中,在一定条件下发生反应:3A(g)+B(g) 2C(g)+xD(g),经5min达到平衡,此时生成2 mol C,测得D的平均反应速率为0.15 mol/(L·min),则平衡时A的物质的量浓度是____________;B的转化率是__________;x的值是___________。
2C(g)+xD(g),经5min达到平衡,此时生成2 mol C,测得D的平均反应速率为0.15 mol/(L·min),则平衡时A的物质的量浓度是____________;B的转化率是__________;x的值是___________。
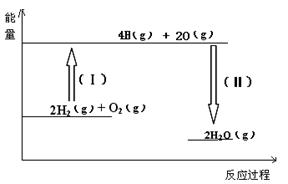
(2)反应2H2(g) + O2 (g)= 2H2O(g) 的能量变化如图所示。已知拆开1molH2、1molO2和1molH-O中的化学键分别需要消耗436KJ、496KJ和463KJ能量,则该反应 (填“吸收” 或“放出”) KJ热量。

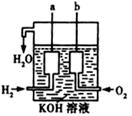
(3)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如右图所示:
a、b两个电极均由多孔的碳块组成。写出a极的电极反应式: 。

(4)工业上用电解饱和食盐水的方法制取金属氯气,反应中能量的转化形式是 ;氯气在 极上产生,反应后溶液的pH 。 (填“增大”或“减小”)。
(9分,每空各1分) (1)0.75mol/L 20% 3 (2)放出 484
(3)H2 +2OH--2e-=2H2O (4)电能转化为化学能 阳 增大
【解析】(1)D的平均反应速率为0.15 mol/(L·min),所以生成物B平衡时物质的量是0.15 mol/(L·min)×5min×4L=3mol,因为物质的量的变化量就是相应的化学计量数之比,所以x=3.消耗AB的物质的量分别是3mol和1mol,因此平衡时A的浓度是(6mol-3mol)÷4L=0.75mol/L,B的转化率是1÷5×100%=20%。
(2)反应热就是断键吸收的能量和形成化学键所放出的能量的差值,所以该反应放出的能量是2×2×463KJ-2×436KJ-496KJ=484KJ。
(3)a极通入的是空气,所以是负极,又因为电解质溶液是氢氧化钾,所以负极反应式为H2 +2OH--2e-=2H2O 。
(4)电解是把电能转化为化学能的装置。电解池中阴离子在阳极放电,所以阳极产生氯气。阴极是氢离子放电,产生氢气。所以溶液中产生氢氧化钠,显碱性,pH增大。


 2C(g)+xD(g),经5min达到平衡,此时生成2 mol C,测得D的平均反应速率为0.15 mol/(L·min),则平衡时A的物质的量浓度是____________;B的转化率是__________;x的值是___________。
2C(g)+xD(g),经5min达到平衡,此时生成2 mol C,测得D的平均反应速率为0.15 mol/(L·min),则平衡时A的物质的量浓度是____________;B的转化率是__________;x的值是___________。