题目内容
13.0.1molNa2SO4溶解在多少mol水中,才能使每100个水分子中含有一个Na+离子( )| A. | 5mol | B. | 10mol | C. | 20mol | D. | 30mol |
分析 每100个水分子中含有一个Na+离子,则水与钠离子的物质的量之比为100:1,0.1molNa2SO4含有0.2molNa+,以此解答.
解答 解:0.1molNa2SO4含有0.2molNa+,每100个水分子中含有一个Na+离子,则水与钠离子的物质的量之比为100:1,则水的物质的量为20mol,
故选C.
点评 本题考查物质的量的计算,为高频考点,侧重于学生的分析、计算能力的考查,注意把握物质的构成特点以及相关计算公式的运用,难度不大.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
3.一定温度时,向2.0L恒容密闭容器中充入1.0mol PCl5,发生反应:PCl5(g)?Cl2(g)+PCl3(g)经一段时间后反应达到平衡.反应过程中测得的部分数据见下表:
下列说法正确的是( )
| 反应时间/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A. | 反应在前50 s内的平均速率为v(PCl3)=0.0032 moI•L-l•s-l | |
| B. | 保持其他条件不变,若升高温度,反应重新达到平衡,平衡时c(PCl3)=0.11moI•L-l,则正反应的△H<0 | |
| C. | 相同温度下,若起始时向容器中充入1.0 molPCl5、0.20mol PCl3和0.20 mol Cl2,则反应达到平衡前v(正)<v(逆) | |
| D. | 相同温度下,若起始时向容器中充入1.0mol PCl3、1.0 mol Cl2,则反应达到平衡时PCl3的转化率为80% |
4.饮水安全在人们生活中占有极为重要的地位,某研究小组提取三处被污染的水源进行了分析,给出了如下实验信息:其中一处被污染的水源含有A、B两种物质,一处含有C、D两种物质,一处含有E物质.A、B、C、D、E五种常见化合物都是由下表中的离子形成:
为了鉴别上述化合物,分别进行以下实验,其结果如下所示:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃片);④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀;⑤将B、D两溶液混合,未见沉淀或气体生成.
根据上述实验填空:
(1)写出B、D的化学式:B:KNO3、D:CuSO4.
(2)将含1mol A的溶液与含1mol E的溶液反应后蒸干,仅得到一种化合物,该化合物为Na2CO3 .
(3)写出实验②发生反应的离子方程式:Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-═AlO2-+2H2O.
(4)C常用作净水剂,用离子方程式表示其净水原理:Al3++3H2O=Al(OH)3(胶体)+3H+.
| 阳离子 | k+ Na+ Cu2+ Al3+ |
| 阴离子 | SO42- HCO3- NO3- OH- |
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃片);④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀;⑤将B、D两溶液混合,未见沉淀或气体生成.
根据上述实验填空:
(1)写出B、D的化学式:B:KNO3、D:CuSO4.
(2)将含1mol A的溶液与含1mol E的溶液反应后蒸干,仅得到一种化合物,该化合物为Na2CO3 .
(3)写出实验②发生反应的离子方程式:Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-═AlO2-+2H2O.
(4)C常用作净水剂,用离子方程式表示其净水原理:Al3++3H2O=Al(OH)3(胶体)+3H+.
1.在2L密闭容器中,把2mol X和2mol Y混合,发生如下反应:3X(g)+Y(g)═nP(g)+2Q(g),当反应经2min达到平衡,测得P的浓度为0.8mol/L,Q的浓度为0.4mol/L,则下列判断中,不正确的是( )
| A. | n=4 | |
| B. | X的转化率为60% | |
| C. | X的平衡浓度为0.4mol/L | |
| D. | 2 min内Y的平均速率为0.4mol/(L.min) |
8.下列离子方程式中,不正确的是( )
| A. | Na2S溶液中通入适量H2S:S2-+H2S═2HS- | |
| B. | 氧化铁溶于氢碘酸:Fe2O3+6H-═2Fe3++3H2O | |
| C. | 过量铁粉加入稀HNO3溶液中:3Fe+8H++2NO${\;}_{3}^{-}$═3Fe2++2NO↑+4H2O | |
| D. | NaHSO3溶液显酸性的原因:HSO${\;}_{3}^{-}$+H2O?SO${\;}_{3}^{2-}$+H3O- |


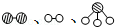 分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是N2、H2被吸附在催化剂表面、在催化剂表面N2、H2中的化学键断裂.
分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是N2、H2被吸附在催化剂表面、在催化剂表面N2、H2中的化学键断裂.