题目内容
(1)24.8g Na2R 含有Na+0.8mol,则R的摩尔质量为
(2)质量都为a g的镁和铝,物质的量之比为 ;将它们分别放入适量的盐酸溶液中恰好完全反应,则消耗的HCl的物质的量之比为 .
(3)在标准状况下,CO和CO2混合气体的质量为36g,体积为22.4L,则其中CO2所占的体积为 ,CO所占的质量为 .
(2)质量都为a g的镁和铝,物质的量之比为
(3)在标准状况下,CO和CO2混合气体的质量为36g,体积为22.4L,则其中CO2所占的体积为
考点:物质的量的相关计算
专题:计算题
分析:(1)24.8g Na2R 含有Na+0.8mol,则Na2R的物质的量为0.4mol,Na2R的摩尔质量=
=62g/mol,结合钠元素的摩尔质量计算R的摩尔质量;
(2)根据n=
计算其物质的量之比;根据金属和酸之间的关系式计算;
(3)混合气体的物质的量=
=1mol,根据质量、物质的量列方程式计算.
| 24.8g |
| 0.4mol |
(2)根据n=
| m |
| M |
(3)混合气体的物质的量=
| 22.4L |
| 22.4L/mol |
解答:
解:(1)24.8g Na2R 含有Na+0.8mol,则Na2R的物质的量为0.4mol,Na2R的摩尔质量=
=62g/mol,则R的摩尔质量=62g/mol-23g/mol×2=16g/mol,
故答案为:16g/mol;
(2)根据n=
知,等质量ag时,镁和铝的物质的量之比=
:
=9:8;根据Mg---2HCl、Al---3HCl知,消耗酸的物质的量之比=(9×2):(8×3)=3:4,故答案为:9:8;3:4;
(3)混合气体的物质的量=
=1mol,设CO和CO2的物质的量分别是xmol、ymol,
,解得
,
二氧化碳体积=0.5mol×22.4L/mol=11.2L,CO的质量=28g/mol×0.5mol=14g,
故答案为:11.2L;14g.
| 24.8g |
| 0.4mol |
故答案为:16g/mol;
(2)根据n=
| m |
| M |
| ag |
| 24g/mol |
| ag |
| 27g/mol |
(3)混合气体的物质的量=
| 22.4L |
| 22.4L/mol |
|
|
二氧化碳体积=0.5mol×22.4L/mol=11.2L,CO的质量=28g/mol×0.5mol=14g,
故答案为:11.2L;14g.
点评:本题考查了物质的量的计算,明确物质的量的有关公式并灵活运用公式解答问题是解本题关键,知道各个物理量之间的关系,题目难度不大.

练习册系列答案
相关题目
X、Y、Z、W、M均为短周期元素,X、Y同主族,X的氢化物和最高价氧化物的水化物能反应生成一种离子化合物,其水溶液显酸性;Z、W、M是第3周期连续的三种元素,其中只有一种是非金属,且原子半径Z>W>M.下列叙述准确的是( )
| A、X、M两元素氢化物的稳定性:X<M |
| B、Z、W、M的氧化物均可做耐高温材料 |
| C、Z是海水中含量最高的金属元素,W是地壳中含量最多的金属元素 |
| D、Z、W、M的单质均能与稀硫酸反应制取氢气,但反应剧烈程度依次减弱 |
关于NaHCO3分类错误的是( )
| A、属于碱类 |
| B、属于碳酸盐类 |
| C、属钠盐类 |
| D、属于化合物类 |

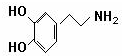 快乐是什么?专家通过实验发现:在大脑的相应部位--“奖赏中心”,给予柔和的电击,便会处于似乎极度快乐的状态.人们已经将“奖赏中心”各部分的脑电图绘制出来,并认为,在各区域之间传递信息的化学物质是多巴胺,所以“奖赏中心”又称为多巴胺系统.多巴胺结构如图:
快乐是什么?专家通过实验发现:在大脑的相应部位--“奖赏中心”,给予柔和的电击,便会处于似乎极度快乐的状态.人们已经将“奖赏中心”各部分的脑电图绘制出来,并认为,在各区域之间传递信息的化学物质是多巴胺,所以“奖赏中心”又称为多巴胺系统.多巴胺结构如图: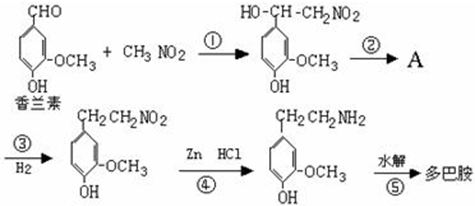
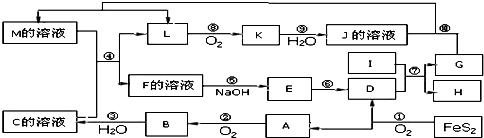
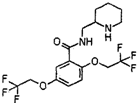 ,它可由龙胆酸(
,它可由龙胆酸(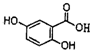 ,为原料合成,合成的方法如图:
,为原料合成,合成的方法如图: