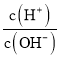��Ŀ����
����Ŀ������ﮣ�LiMn2O4)����������ӵ�س��õ��������ϡ���ҵ�������̿�Ϊԭ�Ͽ��Ʊ�����ﮣ�ͬʱ�Ƶø���ƷMnSO4��H2O���壬��������ͼ��ʾ��
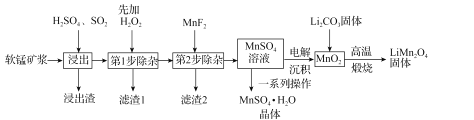
��֪����1�����̿���Ҫ�ɷ�ΪMnO2��������Fe2O3��MgO��Al2O3��CaO��SiO2�����ʡ�
��2���¶ȸ���27��ʱ��MnSO4������ܽ�����¶����߶����͡�
��3���й����ʵ��ܶȻ��������±���
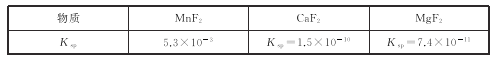
��1����������������MnO2ת��ΪMn2+�����ӷ���ʽΪ_____���ù����У�Ϊ������̿���MnO2�Ľ����ʣ����д�ʩ���е���_____������ĸ����
A�����Ͻ��裬ʹSO2�����̿�ֽӴ�
B������ͨ��SO2������
C���ʵ�����
D���������̿Ľ�����
��2����1�������м���H2O2��Ŀ����_____��
��3����2�����ӣ���Ҫ�ǽ�Ca2+��Mg2+ת��Ϊ��Ӧ�ķ����������ȥ������MnF2��ȥMg2+��Ӧ�����ӷ���ʽΪMnF2(s)+Mg2+(aq)=Mn2+(aq)+MgF2(s)���÷�Ӧ��ƽ�ⳣ��Ϊ_____��
��4��ͼ�е�һϵ�в���ָ����_____��
��5����MnO2��Li2CO3��4��1�����ʵ���֮�����ϣ���Ͻ��裬Ȼ���������600~750�棬��ȡ��ƷLiMn2O4��д���÷�Ӧ�Ļ�ѧ����ʽ��_____��
���𰸡�MnO2+ SO2= SO42-+ Mn2+ AC ��Fe2+����ΪFe3+ 7.2��107 ����Ũ�������ȹ��� 8MnO2+2Li2CO3![]() 4LiMn2O4+2CO2��+O2��
4LiMn2O4+2CO2��+O2��
��������
(1) MnO2��SO2����������ԭ��Ӧ��ת��ΪMn2+��MnO2�Ľ����ʸ��ݷ�Ӧ���������
(2) H2O2 ���������ԣ������ɷ�����
(3) MnF2��ȥMg2+�����ӷ�Ӧ����ʽ��MnF2+ Mg2+![]() Mn2++ MgF2���÷�Ӧ��ƽ�ⳣ����ֵΪ
Mn2++ MgF2���÷�Ӧ��ƽ�ⳣ����ֵΪ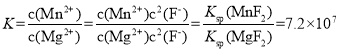 ��
��
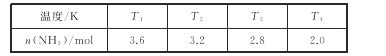
(4) MnSO4������ܽ�����¶����߶����ͣ�Ҫע��������
(5) MnO2��Li2CO3��һ���¶��·�����Ӧ������LiMn2O4��CO2��O2���ݴ˷������
(1)��������������MnO2��SO2����������ԭ��Ӧ��ת��ΪMn2+�����ӷ���ʽΪMnO2+ SO2= SO42-+ Mn2+�� MnO2�Ľ����ʣ�A�����Ͻ��裬ʹSO2�����̿�ֽӴ�������SO2�ͻ����ת��ΪSO42-��A����ȷ��
B������ͨ��SO2�����٣����ܻᵼ�²���SO2δ���ü���Ӧ���ݳ������ʵIJ��ʽ��ͣ�B�����
C���¶����ߣ�����������ӦЧ�ʣ�C����ȷ��
D���������̿Ľ�������SO2���ܲ��ܼ�ʱ�μӷ�Ӧ�����»����ʽ��ͣ�D����ʺ���ѡ����AC���ʴ�ΪMnO2+ SO2= SO42-+ Mn2+��AC��
(2)��1�������м���H2O2��Ŀ���ǽ���Һ�е�Fe2+����ΪFe3+���Ա����γ�Fe(OH)3���������˽�������ȥ���ʴ�Ϊ����Fe2+����ΪFe3+��
(3)MnF2��ȥMg2+�����ӷ�Ӧ����ʽ��MnF2+ Mg2+![]() Mn2++ MgF2���÷�Ӧ��ƽ�ⳣ����ֵΪ
Mn2++ MgF2���÷�Ӧ��ƽ�ⳣ����ֵΪ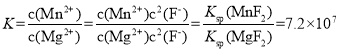 ���ʴ�Ϊ��7.2��107��
���ʴ�Ϊ��7.2��107��
(4)��Һ�����壬ͬʱMnSO4��H2O��ˮ�е��ܽ�����¶ȵ����߶���С����������Ũ�������ȹ��˲������ʴ�Ϊ������Ũ�������ȹ��ˣ�
(5) MnO2��Li2CO3��Ӧ��ֻ��Mn�ļ�̬���ͣ���Ȼ��Ԫ�صĻ��ϼ����ߣ�CԪ�ش������̬���������ߣ���ֻ����OԪ�ؼ�̬���ߣ����Ի���O2���ɡ����ݵ����غ㡢ԭ���غ㣬�ɵø÷�Ӧ�ķ���ʽΪ��8MnO2+2Li2CO3![]() 4LiMn2O4+2CO2��+O2�����ʴ�Ϊ��8MnO2+2Li2CO3
4LiMn2O4+2CO2��+O2�����ʴ�Ϊ��8MnO2+2Li2CO3![]() 4LiMn2O4+2CO2��+O2����
4LiMn2O4+2CO2��+O2����

����Ŀ�������£���ijһԪ��HA��NaOH��Һ�������ϣ�ʵ����Ϣ���£�
ʵ���� | c(HA)/ mol��L��1 | c(NaOH)/ mol��L��1 | ��Ӧ����ҺpH |
�� | 0.1 | 0.1 | pH��9 |
�� | c1 | 0.2 | pH��7 |
�����жϲ���ȷ����
A.c1һ������0.2 mol��L��1
B.HA�ĵ��뷽��ʽ��HA![]() H����A��
H����A��
C.��Ӧ����Һ�У�c(Na��) �� c(OH��)�� c(A��) �� c(H��)
D.�ҷ�Ӧ����Һ�У�c(Na��) �� c(HA)��c(A��)
����Ŀ��25��ʱ��Ũ�Ⱦ�Ϊ0.1mol/L����Һ����pH���±���ʾ���й�˵����ȷ���ǣ� ��
��� | �� | �� | �� | �� |
��Һ | NaCl | CH3COONH4 | NaF | CH3COONa |
pH | 7.0 | 7.0 | 8.1 | 8.9 |
A.����ǿ����CH3COOH>HF
B.���ӵ���Ũ�ȣ���>��
C.����c(CH3COO-)=c(NH4+)=c(OH-)=c(H+)
D.�ں͢���c(CH3COO-)���