题目内容
13.下列说法正确的是( )| A. | 因为合金在潮湿的空气中易形成原电池,所以合金耐腐蚀性都较差 | |
| B. | 常温下2S2O(g)=3S(s)+SO2(g)能自发进行,可推断该反应为放热反应 | |
| C. | 对于反应①C+CO2?2CO(△H>0)和反应②N2+3H2?2NH3(△H<0),达平衡后,升高温度,①反应速率加快,②反应速率减慢 | |
| D. | NH4Cl和HCl溶于水后滴加石蕊都变红色,说明它们均能电离出H+ |
分析 A.不是所有的合金耐腐蚀都很差,根据不同合金的材料和性能解答;
B.依据反应自发进行的判断依据:△H-△S<0解答;
C.温度升高反应速率加快,温度降低反应速率减慢;
D.NH4Cl是强酸弱碱盐,溶于水铵根离子水解生成氢离子.
解答 解:A.不是所有的合金耐腐蚀都很差,例如钛合金、铝合金等具有很好的抗腐蚀性能,故A错误;
B.由方程式2S2O(g)═3S(s)+SO2(g)可知该反应△S<0,要使△H-△S<0,必须满足△H<0,故B正确;
C.温度降低反应速率减慢,升高温度,反应速率加快,①②反应速率均加快,故C错误;
D.氯化铵电离生成铵根离子和氯离子,铵根离子水解生成氢离子,故D错误;
故选B.
点评 本题考查了金属的腐蚀与防护,反应速率的影响因素,反应方向判据,盐类的水解,考查学生对基本知识的掌握程度,题目简单,属于基础题.

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案 期末好成绩系列答案
期末好成绩系列答案
相关题目
3.已知:SO32-+I2+H2O═SO42-+2H++2I-,某溶液中可能含有I-、NH4+、Cu2+、SO32-,向该无色溶液中加入少量溴水,溶液仍呈无色,则下列判断正确的是( )
| A. | 肯定不含I- | B. | 肯定不含NH4+ | C. | 可能含有SO32- | D. | 可能含有I- |
1.下列说法正确的是( )
| A. | 形成离子键的阴阳离子只存在静电吸引力 | |
| B. | 元素周期律是元素的原子核外电子排布周期性变化的结果 | |
| C. | 第三周期非金属元素含氧酸的酸性从左到右依次增加 | |
| D. | 离子化合物中只能含离子键、极性共价键 |
8.有关化学用语正确的是( )
| A. | 质子数27的钴-60原子:60 27Co | |
| B. | 氯化铵的电子式: | |
| C. | S2-的结构示意图: | |
| D. | Cl-的电子排布式:1s22s22p63s23p5 |
18. 阅读、分析下列两个材料:
阅读、分析下列两个材料:
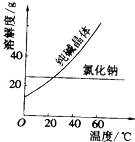
材料一(如图):
材料二:
选择回答下列问题(填写序号):A.分液法 B.“溶解成热饱和溶液、冷却结晶、过滤”的方法 C.“溶解、蒸发结晶、趁热过滤”的方法 D.蒸馏法 E.过滤法 F.萃取法
①将乙二醇和丙三醇相互分离的最佳方法是D.
②提取碘水中的碘,可综合选用上述三种方法依次是F、A、D.
③将含有氯化钠杂质的纯碱提纯出来,最好应用B.
 阅读、分析下列两个材料:
阅读、分析下列两个材料:材料一(如图):
材料二:
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 溶解性 |
| 乙二醇( C2H6O2) | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
| 丙三醇(C3H8O3) | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
①将乙二醇和丙三醇相互分离的最佳方法是D.
②提取碘水中的碘,可综合选用上述三种方法依次是F、A、D.
③将含有氯化钠杂质的纯碱提纯出来,最好应用B.
5.反应物和生成物均为气态的平衡体系,平衡常数表达式为:K=$\frac{c(x)•{c}^{2}(y)}{{c}^{3}(z)•{c}^{2}(w)}$,有关该平衡体系说法不正确的是( )
| A. | 升高温度,该反应平衡常数K的变化无法判断 | |
| B. | 增大压强,W的质量分数减小 | |
| C. | 该反应的化学方程式为:3z(g)+2w(g)?x(g)+2y(g) | |
| D. | 增大X气体浓度平衡向正反应方向移动 |
2.催化剂的研究是化学反应原理中的一个重要领域,下列有关叙述正确的是( )
| A. | 加催化剂可以增大或减小化学反应的焓变 | |
| B. | 催化剂能降低反应所需活化能 | |
| C. | 任何化学反应都需要活化能的推动 | |
| D. | 对于在给定条件下反应物之间能够同时发生多个反应的情况,理想的催化剂可以大幅度提高目标产物在最终产物中的比例 |

