��Ŀ����
����Ŀ����Ȼ����һ����Ҫ�Ļ���ԭ�ϣ����к�������H2S�ʻ���COS��������������ж�����ѧ��Ʒ�����½��ʹ�����Ⱦ��
��1����ˮ��������H2S������������NH4HS��д����Ӧ�����ӷ���ʽ___��
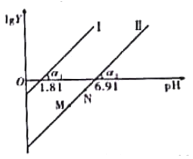
��2�����ú�Fe3+����Һ�����ѳ����е�H2S����H2S�Ϳ�����һ������ͨ����FeCl3��Һ����ʵ�ֿ�������õ�������FeCl3��Һ����H2S�����У���Һ�е�n��Fe3+���������յ�n��H2S����ʱ��t�仯��ͼ��
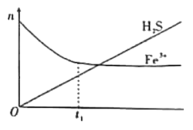
��t1��ǰ����Һ��n��Fe3+�����ϼ�С��ԭ����___�������ӷ���ʽ��ʾ����
��t1�Ժ���Һ��n��Fe3+���������ֲ��䣬ԭ����___����ʱ����Һ���ܷ�Ӧ�����ӷ���ʽ���Ա�ʾΪ___��
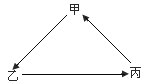
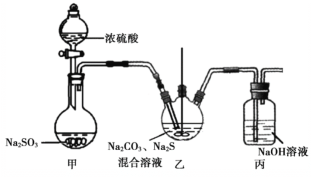
��3���ʻ���ļ���ˮ���dz��õ���������������ͼ��
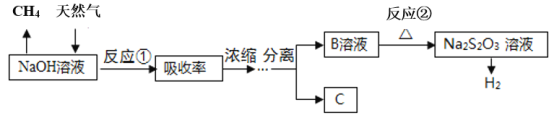
����֪B�����ƣ�C��һ�����Σ���B�ĵ���ʽΪ___��C�Ļ�ѧʽΪ___��
��д����Ӧ�ڵ����ӷ���ʽ___��
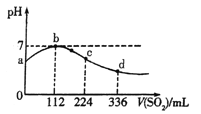
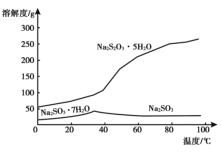
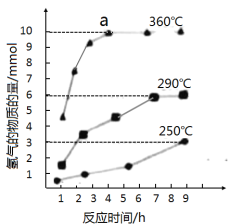
����ͼ�Ƿ�Ӧ���У��ڲ�ͬ��Ӧ�¶���.��Ӧʱ����H2�����Ĺ�ϵ��Na2S��ʼ����Ϊ3mmol������ͼ�������֪��a��ʱ��Һ�г�S2O32-�⣬����___������������ӷ��ţ���
���𰸡�H2S+NH3��H2O=NH4++HS-+H2O 2Fe3++H2S=2Fe2++S��+2H+ t1�Ժ���Һ��ͬʱ����������Ӧ��Fe3+��������H2S��Fe2+��O2��������Fe3+����������Ӧ�������ʱ����Һ��n(Fe2+)���ֻ������� 2H2S+O2![]() 2S��+2H2O
2S��+2H2O ![]() Na2CO3 2S2-+5H2O
Na2CO3 2S2-+5H2O![]() S2O32-+4H2��+2OH- SO42-
S2O32-+4H2��+2OH- SO42-
��������
Fe3+��H2S����������ԭ��Ӧ����Fe2+��S��ͬʱFe2+����������������ΪFe3+����Ȼ���е��ʻ���COS�����������Ʒ�Ӧ�������ƣ��Ƿ�������ԭ��Ӧ��C��һ�����Σ��Ʋ�CΪ̼���ƣ����Ʒ���������ԭ��Ӧ������S2O32-��SO42-�������������ʡ�
��1����ˮ�е�һˮ�ϰ���H2S��Ӧ�кͷ�Ӧ������NH4HS�����ӷ���ʽΪH2S+NH3��H2O=NH4++HS-+H2O��
��2������ͼ��֪��t1ǰn��Fe3+��Ѹ�ټ�С�������յ�n��H2S���������ӣ����������ӷ�ӦΪ2Fe3++H2S=2Fe2++S��+2H+��
��t1�Ժ���Һ��ͬʱ����������Ӧ��Fe3+��������H2S��Fe2+����������������Fe3+����������Ӧ�������ʱ����Һ��n��Fe3+���������ֲ��䡣t1�Ժ�Fe3+������ã��ܷ�Ӧ����ʽΪ2H2S+O2![]() 2S��+2H2O��
2S��+2H2O��
��3��������Ϊ���ӻ�����������ӡ������ӹ��ɣ������ʽΪ![]() ��COS���������Ʒ�Ӧǰ�ϼ�û�б仯�����ɺ���+4��̼Ԫ�ص����Σ�������Ϊ̼���ƣ��䷴Ӧ����ʽΪCOS+4NaOH=Na2S+Na2CO3+2H2O��
��COS���������Ʒ�Ӧǰ�ϼ�û�б仯�����ɺ���+4��̼Ԫ�ص����Σ�������Ϊ̼���ƣ��䷴Ӧ����ʽΪCOS+4NaOH=Na2S+Na2CO3+2H2O��
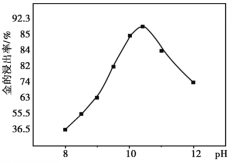
��ͼʾ˵����������Һ����������Na2S2O3������������������ԭ��Ӧ�����ݵ�ʧ�����غ�͵���غ���ƽ�������ӷ���ʽΪ2S2-+5H2O![]() S2O32-+4H2��+2OH-��
S2O32-+4H2��+2OH-��
�۸���ͼ���֪��a��ʱ������10mol��˵����Ӧ�й���20mol���ӷ���ת�ƣ�����ݵ�ʧ�����غ��֪��3mol���Ʒ��ӱ����ṩ20mol���ӣ�ȫ��ת��Ϊ���������ת��12mol���ӣ�ȫ��ת��Ϊ��������ת��18mol���ӣ�ȫ��ת��Ϊ������ת��24mol���ӣ�����a��ʱ��Һ�г�S2O32-�⣬����SO42-��