��Ŀ����
����Ŀ��Na2S2O3Ӧ�ù㷺��ˮ�����г�������ԭ����ұ���г�������ϼ���
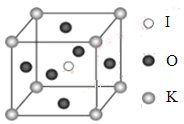
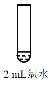
(1)Na2S2O3��ʵ�����Ʒ���װ����ͼ�����Ⱥͼг�װ���ԣ���

��֪��2Na2S + 3SO2 = 2Na2SO3 + 3S�� ��Na2SO3 + S = Na2S2O3
�ټ��з�����Ӧ�Ļ�ѧ����ʽΪ______��
��ʵ������У����еij�����Һ�ȱ���ǣ�������ʱ���ɴ�����Na2S2O3��һ��ʱ��������ٴγ����������ǣ���ʱ������ֹͣͨ��SO2��������ӷ���ʽ���ʹ�ʱ��������ֹͣͨ��SO2��ԭ��______��

�۱��У�NaOH��Һ���յ����������______��
(2)ʵ�ʹ�ҵ�������Ƶõ�Na2S2O3��Һ�г���������Na2SO3������ܽ�����ߣ���ͼ�������Na2S2O35H2O�ķ�����______��
(3)Na2S2O3����;��������������μ��Ƚ�����һ�ֻ����ѺõĻƽ�Au����ȡ���ա�
��֪��I. Cu(NH3)42+=Cu2++4NH3��
II. Cu2+�ڼ��Խ�ǿʱ���Ȼ�����CuO������
�ٽ����ʯ������Na2S2O3��Cu(NH3)42+�Ļ����Һ�У���ͨ��O2������Ӧ��ԭ��Ϊ��
i.Cu(NH3)42+ + Au + 2S2O32![]() Cu(NH3)2+ + Au(S2O3)23+ 2NH3
Cu(NH3)2+ + Au(S2O3)23+ 2NH3
ii.4Cu(NH3)2+ + 8NH3+ O2 + 2H2O = 4Cu(NH3)42+ + 4OH
�������Cu(NH3)42+���������ã����ܷ�Ӧ�����ӷ���ʽΪ��______��

�� һ���¶��£���ͬʱ���Ľ���������ϵpH�仯��������ͼ������pH��10.5ʱ����Ľ����ʽ��͵Ŀ���ԭ��_______����д��2�㼴�ɣ�
���𰸡�Na2SO3 +H2SO4=Na2SO4+ SO2 ��+ H2O ������SO2����ˮʹ��Һ������ǿ��S2O32-+2H2SO3 =S��+ SO2��+ H2O +2HSO3-��S2O32- +2H+= S��+ SO2��+ H2O SO2��H2S����CO2 ����Һ����Ũ����(���ȹ���)�����½ᾧ�����ˡ� 4Au + 8S2O32- + O2 + 2H2O = 4Au(S2O3)23- + 4OH-�����Խ�ǿʱ���ɵ�CuO���������ڽ��ʯ���棬���ͣ���������Ӧ���� pH��10.5ʱ������Cu(NH3)42+ת����CuO��������Cu(NH3)42+Ũ�ȣ����ͣ���������Ӧ���ʡ����Խ�ǿʱ��������S2O32-���������ͣ���������Ӧ���ʡ�
��������
�������ṩ���Ʊ���������Ƶķ�Ӧ����ʽ�Լ�װ��ͼ��֪����Ҫ�ɼ�װ���Ʊ�SO2������ͨ����װ���з�Ӧ�ſɣ���������ʢ�ŵ���̼���ƺ����ƵĻ����Һ����H2SO3�����Ա�H2CO3��H2S��ǿ����������װ����Ҳ���ܻᷢ����Ӧ����CO2��H2S���壻���ǵ�SO2�����п�������Ӧ��ȫ�������װ�õij���������ܺ���SO2��CO2�Լ�H2S������б�Ҫ���ñ�װ�ö�β�����д������Ӻ��������������ʵ������������Һ�л��Na2S2O3��5H2O�����Ǿ������ʱ��Ҫ������и������ܽ�����߽��з���������Na2SO3�ڽϸ��¶�ʱ�ܽ�Ƚ�С���෴���ǣ�Na2S2O3��5H2O�ڽϸ��¶�ʱ�ܽ�Ƚϴ������Ҫ�Ƚ���Һ����Ũ�����ڽϸ��¶�ʱ�����ȹ��˵�������Na2SO3���ʣ��ٶ���Һ���£�ʹNa2S2O3��5H2O�ᾧ���������˼��ɡ�����д�ƽ��ȡ���ܷ�Ӧ����ʽʱ��Ҫע��![]() ��������Ӧ������������Ǵ����ã���ˣ��ܷ�Ӧ����ʽ�в�δ���ĺ�����
��������Ӧ������������Ǵ����ã���ˣ��ܷ�Ӧ����ʽ�в�δ���ĺ�����![]() ��ʵ����Au��O2֮���������ԭ��Ӧ���ڷ���������������εȽ��лƽ��ȡʱpH���ߵ������½�ȡ�ʽϵ͵�ԭ��ʱ��Ҫע�����и����Ĺ���
��ʵ����Au��O2֮���������ԭ��Ӧ���ڷ���������������εȽ��лƽ��ȡʱpH���ߵ������½�ȡ�ʽϵ͵�ԭ��ʱ��Ҫע�����и����Ĺ���![]() �Լ�Cu2+�ķ�Ӧ���ʡ�
�Լ�Cu2+�ķ�Ӧ���ʡ�
(1)��ͨ��������֪����װ����������SO2����˷�Ӧ�Ļ�ѧ����ʽΪ��![]() ��
��
�ڽ����Ŀ���ṩ���Ʊ���������Ƶķ���ʽ�������Ʊ����������е���Һ�ȱ���ǣ�����Ϊ������S���ʣ�S���ʼ������������Ʒ�Ӧ����Na2S2O3�������Һ�ֱ���壻������ͨSO2�����ڻ�����H2SO3��������Һ�����Ի���ǿ����Һ�ٴγ��ֻ��ǣ�˵��S�����ٴ����ɣ���ôԭ����ǣ�Na2S2O3��������������·����ֽ⣬������S���ʣ���ص����ӷ���ʽΪ��![]() ��
��
��ͨ��������֪����װ���г�����������ܺ���SO2��CO2��H2S�����NaOH��Һ���յ����������SO2��CO2��H2S��
(2)ͨ��������֪���Ӻ��������������ʵ������������Һ�л��Na2S2O3��5H2O����Ҫ�Ƚ���Һ����Ũ�����ڽϸ��¶�ʱ�����ȹ��˵�������Na2SO3���ʣ��ٶ���Һ���£�ʹNa2S2O3��5H2O�ᾧ�������ٽ��й��˼��ɣ�
(3)�������֪��![]() ��������Ӧ������������Ǵ����ã���ˣ��ܷ�Ӧ��δ���ĺ�����
��������Ӧ������������Ǵ����ã���ˣ��ܷ�Ӧ��δ���ĺ�����![]() ���ܷ�Ӧʵ����Au��O2֮���������ԭ��Ӧ������ܷ�Ӧ�����ӷ���ʽΪ��
���ܷ�Ӧʵ����Au��O2֮���������ԭ��Ӧ������ܷ�Ӧ�����ӷ���ʽΪ��![]() ��
��
��ͨ��������֪������̫ǿ��Ľ������½���ԭ������ǣ�pH��10.5ʱ������![]() ת����CuO��������
ת����CuO��������![]() Ũ�ȣ��Ӷ�ʹ�������½��������Ǽ��Խ�ǿʱ��������
Ũ�ȣ��Ӷ�ʹ�������½��������Ǽ��Խ�ǿʱ��������![]() �������Ӷ����½������½���
�������Ӷ����½������½���

 ȫ��������ϵ�д�
ȫ��������ϵ�д�����Ŀ��ѧϰС��̽��AgNO3��Ag2O(�غ�ɫ���壬������ˮ)����ˮƯ���Ե�Ӱ�졣
ʵ���¼���£�
| ʵ�� | ���������� |
�� | ����1mL����ˮ���ٵμ�1��Ʒ����Һ��Ʒ����Һ�Ͽ���ɫ | |
�� | ��������Ag2O���壬������ɫ����a���ټ���1mL����ˮ�� 1��Ʒ����Һ��Ʒ����Һ��ɫ��i�� | |
�� | ����1mL��ŨAgNO3��Һ��������ɫ����b���ٵμ�1��Ʒ����Һ��Ʒ����Һ��ɫ��i�� |
(1)�����ӷ���ʽ��ʾi��Ʒ����Һ��ɫ��ԭ��______��
(2)�����飬ii�еİ�ɫ����a��AgCl������AgCl�Ļ�ѧ����ʽ��_______��
(3)����iii�ĶԱ�ʵ�飬Ŀ�����ų�iii��______��ɵ�Ӱ�졣
(4)�о���ɫ����b�ijɷ֡�����ʵ��iv����ʵ��iii�ķ����ٴεõ���ɫ����b�����ˡ�ϴ�ӣ������Թ��У���
ʵ��iv:
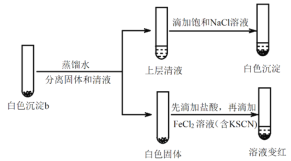
����ƶԱ�ʵ��֤ʵ��ɫ����b��ֻ����AgCl��ʵ�鷽����������_______��
��FeCl2��Һ��������_______���ɴ��жϣ���ɫ����b���ܺ���AgClO��
(5)��һ���о���ɫ����b��ʵ��iiiƷ����Һ��ɫ����ԭ����ʵ��v��
ʵ��v:

�ٽ�����ӷ���ʽ���ͼ��뱥��NaCl��Һ��Ŀ�ģ�_______��
���Ʋ�Ʒ����Һ��ɫ�����ʣ�ʵ��iii��ʵ��v______����족�� ����������