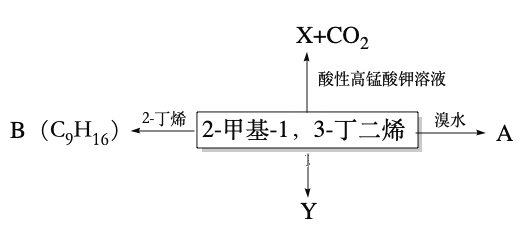
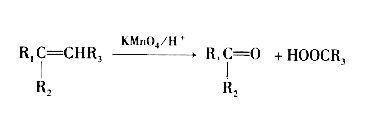
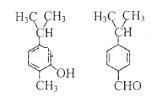
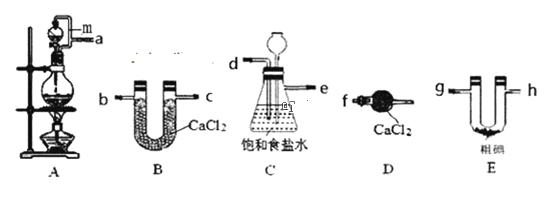
题目内容
【题目】X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示,若W原子的最外层电子数是内层电子总数的![]() ,下列说法中正确的是
,下列说法中正确的是

A.阴离子的半径从大到小排列顺序为 X>Y>Z>W
B.X、Y、Z、W 元素的氢化物分子间都可以形成氢键
C.Y 的两种同素异形体在常温下可以相互转化
D.最高价氧化物对应的水化物的酸性:W>Z
【答案】D
【解析】
W原子的最外层电子数是内层电子总数的![]() ,应为Cl,由元素在周期表中的位置可知X为N元素,Y为O元素,Z为S元素,据此分析结合元素性质解答。
,应为Cl,由元素在周期表中的位置可知X为N元素,Y为O元素,Z为S元素,据此分析结合元素性质解答。
根据分析,W为Cl元素,X为N元素,Y为O元素,Z为S元素,
A.同周期元素随核电荷数增大半径逐渐减小,原子核外电子层数越多,离子半径越大,应为Z>W>X>Y,故A错误;
B.S、Cl的非金属性较弱,氢化物分子间不存在氢键,故B错误;
C.Y为O,对应的两种同素异形体分别为O2、O3,在放电条件下可以相互转化,故C错误;
D.W为Cl元素,Z为S元素,元素的非金属性越强,对应的最高价氧化物对应的水化物的酸性越强,非金属性Cl>S,最高价氧化物对应的水化物的酸性:W>Z,故D正确;
答案选D。

 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案【题目】卤族元素在生活中有广泛应用,根据所需知识回答下列问题。
(1)氟元素基态原子的价电子排布图:_________,卤族元素位于元素周期表______区。
(2)在一定浓度的氢氟酸溶液中,部分溶质以二分子缔合(HF)2形式存在,使HF分子缔合的作用力是_______________。
(3)BF3常温下是气体,有强烈的接受弧电子对的倾向。BF3分子的立体构型为______,固态时的晶体类型是_______,BF3与NH3相遇立即生成白色固体,写出该白色固体物质的结构式并标注出其中的配位键_____。
(4)根据下表提供的数据判断,熔点最高、硬度最大的是_______(填化学式)。
离子晶体 | NaF | MgF2 | AlF3 |
晶格能(KJ·mol-1) | 923 | 2957 | 5492 |
(5)已知NaClO2晶体中阴离子为V型,ClO2-中氯原子的弧电子对数是______,ClO2-中氯原子的杂化轨道类型为_____,HClO4比HClO2酸性强的原因是_______。
(6)CaF2晶胞如下图所示。已知:NA为阿伏伽德罗常数,棱上相邻的两个Ca2+的核间距为acm,则CaF2的密度可表示为_____g·cm-3。

【题目】在标准状况下进行甲、乙、丙三组实验。三组实验各取同浓度的盐酸30mL,加入同一种镁铝合金粉末,产生气体。有关数据列表如下(气体体积均为标准状况下测得):
实验序号 | 甲 | 乙 | 丙 |
合金质量/mg | 255 | 385 | 459 |
气体体积/mL | 280 | 336 | 336 |
(1)乙组实验中,盐酸_____________(填“过量”、“适量”或“不足量”),理由是_________。
(2)要计算盐酸的物质的量浓度,题中可做计算依据的是____。
(3)合金中Mg、Al的物质的量之比为_________________。
(4)在丙组实验后,向容器中加入1mol/L的NaOH溶液,能使合金中的铝恰好溶解,不形成铝的沉淀,并使Mg2+刚好沉淀完全,求所加NaOH溶液的体积。(写出计算过程)_____________