题目内容
【题目】下列关于物质的量浓度表述正确的是( )
A.0.2mol·L-1Na2SO4溶液中含有Na+和SO42-总物质的量为0.6mol
B.50mL 2mol·L-1的NaCl溶液和100 mL L 0.5mol·L-1MgCl2溶液中,Cl-的物质的量浓度相等
C.用1L水吸收22.4L氯化氢(标况下)所得盐酸的浓度是1mol·L-1
D.10g 98%的硫酸(密度为1.84g·cm-3)与10mL 18.4mol·L-1的硫酸的浓度是相同的
【答案】D
【解析】A.不知道体积,无法计算Na+的物质的量,A不符合题意;
B.物质的量浓度和溶液的体积没有关系,50mL 2mol·L-1的NaCl溶液和100 mL L 0.5mol·L-1MgCl2溶液中,Cl-的物质的量浓度不相等,B不符合题意;
C.溶液的体积为1L而不是溶剂的体积为1L,用1L水吸收22.4L氯化氢(标况下)所得盐酸的体积不是1L,C不符合题意;
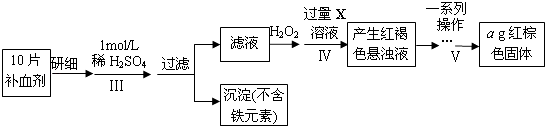
D.根据公式c= ![]() =18.4mol/L,D符合题意。
=18.4mol/L,D符合题意。
所以答案是:D。
【考点精析】解答此题的关键在于理解物质的量浓度的概念的相关知识,掌握以单位体积里所含溶质B的物质的量来表示溶液组成的物理量,叫做溶质B的物质的量浓度;符号CB=nB(mol)/V(L) (nB是溶质B的物质的量,V是溶液体积),单位是mol·Lˉ1.

练习册系列答案
相关题目