题目内容
【题目】发展“碳一化学”,开发利用我国丰富的煤炭资源具有重要的战略意义和经济价值。请回答下列问题:
(1)已知:常温下C(s)的燃烧热△H=-393.5 kJ·mol-1, S(s)的燃娆热△H=-296.0 kJ·mol-l ,CO2(g)+C(S)=2CO(g) △H=+172.5 kJ·mol-1,写出一氧化碳将二氧化硫还原为单质硫的热化学方程式:______
(2)在763 K、3.04×104 kPa时,用CO和H2做原料合成甲醇(CH3OH),存在下列平衡:CO(g)+2H2(g) ![]() CH3OH(g)。当原料中CO和H2的比例不同时,对CO的转化率及平衡混合物中甲醇的体积分数都有影响。
CH3OH(g)。当原料中CO和H2的比例不同时,对CO的转化率及平衡混合物中甲醇的体积分数都有影响。
①设H2和CO起始物质的量之比为m,平衡时CO的转化率为α,平衡混合物中甲醇的体积分数为y,则m、α、y三者的关系式为y=___。
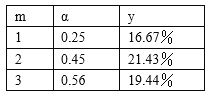
②根据表中提供的数据,可得出反应物的比例对CO的平衡转化率以及平衡混合物中甲醇的体积分数影响的结论,选择最佳反应物配比m=_______(填“l”、“2”或“3”),理由是_________。
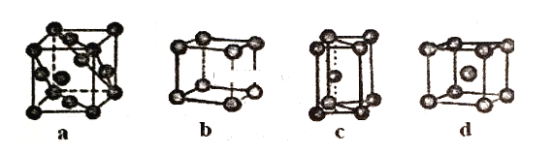
(3)如图是四种金属氧化物被一氧化碳还原,反应达到平衡时lgc(CO)/c(CO2)与温度(T)的关系曲线图:

①8000C时,其中最易被还原的金属氧化物是______(填化学式),该反应的平衡常数K=_______。
②CO2还原PbO2的反应△H ___0(填“>”或“<”)。判断依据是_________。
(4)科学家正在研究用固态物质作为火箭推进剂。固体推进剂(硝酸钾和蔗糖的混合物)点燃后在燃烧室里燃烧,发生反应KNO3+C12H22O11→CO2↑+N2↑+H2O+K2CO3,(未配平)。则该反应中氧化剂与还原剂的物质的量之比是_______。
【答案】2CO(g)+SO2(g)=S(s)+2CO2(g) ΔH=-270 kJmol-1 a/1+m-2a 2 由表中数据可知,m越大,α越大;开始时m增大,y也随着增大,当m>2 时,m增大,y减小,当m=2 时,y最大 Cu2O 1×106 < 温度升高,CO 还原 PbO2 的反应的 lgc(CO)/c(CO2)变大,说明 CO 的转化率变低(或其他合理说法) 48∶5
【解析】
(1)已知:常温下C(s)的燃烧热△H=-393.5 kJ.mol-1,即①C(s)+ O2(g)= CO2(g) △H1=-393.5 kJ.mol-1;
S(s)的燃娆热△H=-296.0 kJ.mol-l ,即②S(s)+ O2(g)= SO2(g) △H2=-296.0 kJ.mol-1;
③CO2(g)+C(s)=2CO(g) △H3=+172.5 kJ .mol-1,
根据盖斯定律,由①-②-③得反应2CO(g)+SO2(g)=S(s)+2CO2(g) ΔH=△H1-△H2-△H3=-393.5 kJ.mol-1+296.0 kJ.mol-1-172.5 kJ .mol-1=-270 kJmol-1;
(2)①设开始时CO为1mol,则H2为mmol,
由: CO+2H2![]() CH3OH
CH3OH
n始/ mol:1 m 0
n变/ mol:a 2a a
n平/ mol:1-a m-2a a
平衡时n(总)=(1+m-2a)mol
故y=![]() ×100%;
×100%;
②根据表中提供的数据,可得出反应物的比例对CO的平衡转化率以及平衡混合物中甲醇的体积分数影响的结论,选择最佳反应物配比m=2,理由是由表中数据可知,m越大,α越大;开始时m增大,y也随着增大,当m>2 时,m增大,y减小,当m=2 时,y最大;
(3)①800℃时,K越大,金属氧化物越易被还原,故Cu2O越易被还原,lgc(CO)/c(CO2)=-6,即lg ![]() =-6,则K= 1×106;
=-6,则K= 1×106;
②CO2还原PbO2的反应△H<0,判断依据是温度升高,CO 还原 PbO2 的反应的 lgc(CO)/c(CO2)变大,说明 CO 的转化率减小;
(4)反应KNO3+C12H22O11→CO2↑+N2↑+H2O+K2CO3中氮元素由+5价变为0价,碳元素由0价变为+4价,根据氧化还原反应配平得反应48KNO3+5C12H22O11=36CO2↑+12N2↑+55H2O+24K2CO3,则该反应中氧化剂KNO3与还原剂C12H22O11的物质的量之比是48:5。

 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案【题目】下列实验操作、现象及结论均正确的是
实验操作、现象 | 结论 | |
A | 取1 mL 20%的蔗糖溶液,加入3~5滴稀硫酸。水浴加热5 min后取少量溶液,加入少量新制Cu(OH)2,加热,无砖红色沉淀产生 | 蔗糖没有发生水解 |
B | 向装有溴水的分液漏斗中加入裂化汽油,充分振荡并静置,下层为橙色 | 裂化汽油可以萃取溴 |
C | 将SO2通入紫色石蕊溶液中,溶液先变红后褪色 | SO2是酸性氧化物,还具有漂白性 |
D | 分别向盛有KI3溶液的a、b试管中滴加淀粉溶液、AgNO3溶液,a中溶液变蓝,b中产生黄色沉淀 | 溶液中存在:I3- |
A. AB. BC. CD. D