题目内容
【题目】某校研究性学习小组的同学在学习了氨的性质后讨论:运用类比的思想,既然氨气具有还原性,能否像H2那样还原CuO呢?他们设计实验制取氨气并探究上述问题。请你参与该小组的活动并完成下列研究:
【制取氨气】
(1)实验室常用加热氯化铵和氢氧化钙固体混合物的方法来制取氨气,该方法制备氨气的装置为_____(填字母,下同),收集氨气的装置可以是__________。
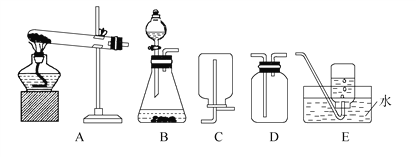
【实验探究】
该小组设计实验探究氨气的还原性及其产物,实验装置图(夹持装置未画出)如下:
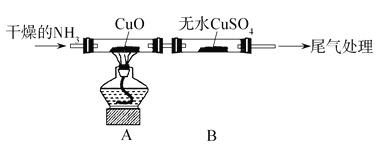
(2)通入的NH3必须干燥的原因是__________________。
(3)实验中观察到CuO变为红色物质,无水CuSO4变蓝,同时生成一种无污染的气体。请写出NH3与CuO反应的化学方程式:_____________________。
【问题讨论】
有同学认为:NH3与CuO反应生成的红色物质中可能含有Cu2O.已知Cu2O是红色粉末,是一种碱性氧化物,在酸性溶液中,Cu+能自身发生氧化还原反应生成Cu2+和Cu.请你设计一个简单的实验检验该红色物质中是否含有Cu2O:____________________。
【答案】 A CD NH3不干燥会影响产物的检验 2NH3+3CuO![]() 3Cu+N2+3H2O 取少量红色固体样品于试管中,向其中加入适量的稀盐酸(或稀盐酸),若观察溶液变成蓝色,说明该样品中含有Cu2O
3Cu+N2+3H2O 取少量红色固体样品于试管中,向其中加入适量的稀盐酸(或稀盐酸),若观察溶液变成蓝色,说明该样品中含有Cu2O
【解析】(1)实验室常用加热氯化铵和氢氧化钙固体混合物的方法来制取氨气,属于固体和答题加热制备气体的反应,则该方法制备氨气的装置为A;氨气极易溶于水,且密度小于空气,因此应该用向下排空气法收集,则收集氨气的装置可以是CD;(2)氨气和氧化铜反应需要干燥的氨气,因此通入的NH3必须干燥的原因是NH3不干燥会影响产物的检验;CuO变为红色物质,说明被还原生成了单质铜。无水CuSO4变蓝色,说明有水生成。同时生成一种无污染的气体,说明氨气被氧化生成氮气,方程式为2NH3+3CuO![]() N2+3Cu+3H2O。(3)在酸性溶液中,Cu+ 的稳定性比Cu2+ 差,(即2Cu+→ Cu+ Cu2+ )。因此可利用生成的Cu2+在溶液中显蓝色来验证,因此检验该红色物质中是否含有Cu2O的实验方案是:取少量红色固体样品于试管中,向其中加入适量的稀盐酸(或稀硫酸),若观察溶液变成蓝色,说明该样品中含有Cu2O。
N2+3Cu+3H2O。(3)在酸性溶液中,Cu+ 的稳定性比Cu2+ 差,(即2Cu+→ Cu+ Cu2+ )。因此可利用生成的Cu2+在溶液中显蓝色来验证,因此检验该红色物质中是否含有Cu2O的实验方案是:取少量红色固体样品于试管中,向其中加入适量的稀盐酸(或稀硫酸),若观察溶液变成蓝色,说明该样品中含有Cu2O。

 名校课堂系列答案
名校课堂系列答案

