题目内容
7.某学生欲配制50g 质量分数为7.0%的氯化钠溶液,在称量氯化钠的操作中,将砝码放在左盘(1g以下使用游码),该学生配制的氯化钠溶液的质量分数偏小(填“偏大”、“偏小”或“不变”),实际是5.1%.分析 利用溶质质量=溶液质量×溶质的质量分数,计算出溶质质量和溶剂质量,根据左盘质量=右盘质量+游码质量,列出等式算出实际称量的质量,再计算出溶质质量分数即可.
解答 解:配制50g质量分数为7.0%的NaCl溶液所需溶质质量为:50g×7.0%=3.5g,需水的质量为:50g-3.5g=46.5g,称量需使用3g的砝码,将游码拨到0.5g刻度处,由左盘质量=右盘质量+游码质量,则3g=氯化钠的质量+0.5g,可得实际称得氯化钠的质量为2.5g,故该学生配制的NaCl溶液的质量分数实际是$\frac{2.5g}{2.5g+46.5g}$×100%=5.1%,质量分数偏小.
故答案为:偏小,5.1%.
点评 本题考查溶液的配制,难度不大,掌握溶质质量分数的有关计算、左盘质量=右盘质量+游码质量是解答本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17.用pH试纸测某溶液的pH时,规范的操作是( )
| A. | 将pH试纸放入溶液,观察其颜色变化,跟标准比色卡比较 | |
| B. | 用干燥洁净的玻璃棒蘸取溶液,滴在pH试纸上,跟标准比色卡比较 | |
| C. | 用蒸馏水湿润pH试纸,用玻璃棒蘸取溶液,滴在pH试纸上,跟标准比色卡比较 | |
| D. | 在试管内放入少量溶液煮沸,把pH试纸放在试管口上观察,跟标准比色卡比较 |
15.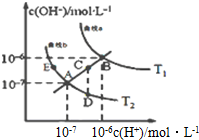 水的电离常数如图两条曲线所示,曲线中的点都符合c(H+)×c(OH-)=常数,下列说法错误的是( )
水的电离常数如图两条曲线所示,曲线中的点都符合c(H+)×c(OH-)=常数,下列说法错误的是( )
 水的电离常数如图两条曲线所示,曲线中的点都符合c(H+)×c(OH-)=常数,下列说法错误的是( )
水的电离常数如图两条曲线所示,曲线中的点都符合c(H+)×c(OH-)=常数,下列说法错误的是( )| A. | 图中温度T1>T2 | |
| B. | 图中五点Kw间的关系:B>C>A=D=E | |
| C. | 曲线a、b可以表示纯水的电离情况 | |
| D. | 若处在B点时,将pH=2的硫酸溶液与pH=11的KOH溶液等体积混合后,溶液显酸性 |
12.下列说法错误的是( )
| A. | 1mol 氢 | B. | 1mol O | C. | 1mol 二氧化碳 | D. | 1mol 水 |
4.下列关于煤、石油、天然气等资源的说法正确的是( )
| A. | 石油裂解得到的汽油是纯净物 | |
| B. | 煤的气化是物理变化 | |
| C. | 天然气是一种清洁的化石燃料 | |
| D. | 水煤气是通过煤的液化得到的气体燃料 |
2.设nA为阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 常温常压下,11.2 L氧气含有的分子数目为nA | |
| B. | 1 mol H2所含有的电子数目为nA | |
| C. | 4.4 g 二氧化碳含有的分子数目为0.1 nA | |
| D. | 1 mol/L CaCl2溶液中含有的氯离子数目为2nA |
 常温下,浓度均为0.1mol•L-1的四种溶液:
常温下,浓度均为0.1mol•L-1的四种溶液: