题目内容
【题目】下列物质不能与氢氧化钠溶液反应的是
A. Al B. Fe2O3 C. Ca(HCO3)2 D. Al(OH)3
【答案】B
【解析】试题分析:A、铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,A错误;B、氧化铁是碱性氧化物,和氢氧化钠溶液不反应,B正确;C、碳酸氢钙和氢氧化钠反应生成碳酸钙、碳酸钠和水,C错误;D、氢氧化铝是两性氢氧化物,和氢氧化钠溶液反应生成偏铝酸钠和水,D错误,答案选B。

 期末冲刺100分创新金卷完全试卷系列答案
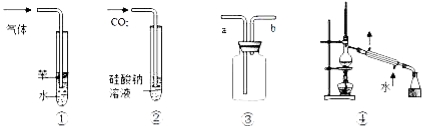
期末冲刺100分创新金卷完全试卷系列答案【题目】某研究小组利用下图装置探究CO还原Fe2O3所得到的一种黑色粉末的成分(固定装置略去)。(已知:Fe2+遇到K3[Fe(CN)6]溶液生成蓝色沉淀)

请回答问題:
(1)按气流方向,各仪器接口从左到右的连接顺序为:
i→____________→____________→g→h→__________→__________→j → k→ ____________→___________。(填字母编号)
(2)证明Fe2O3己被还原的现象是___________________。
(3)研究小组对黑色粉末的成分提出下列猜想:
【猜想一】黑色粉末的成分可能是Fe。
【猜想二】黑色粉末的成分可能是FeO。
【猜想三】黑色粉末的成分可能是__________________。
设计并完成实验如下:
步骤 | 操作 | 现象 |
1 | 加入稀盐酸 | 溶解,无气泡 |
2 | 取步骤1中溶液,滴加K3[Fe(CN)6]溶液 | 蓝色沉淀 |
3 | __________________ | 变红 |
①根据实验现象,则猜想_________成立。
②研究小组又向步骤3的溶液中滴加新制氯水,发现溶液红色褪去。可能的原因及验证方法为__________________。
(4)上述装置还有不妥之处,改进措施为____________________。
【题目】Ⅰ.下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。

(1)下列___________ (填写编号)组成元素的单质可能都是电的良导体。
①a、c、h ②b、g、k ③c、h、i ④d、e、f
(2)如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响:
A.原子核对核外电子的吸引力
B.形成稳定结构的倾向。
Ⅱ.下表是一些气态原子失去核外不同电子所需的能量(kJ·mol-1):
锂 | X | Y | |
失去第一个电子 | 519 | 502 | 580 |
失去第二个电子 | 7 296 | 4 570 | 1 820 |
失去第三个电子 | 11 799 | 6 920 | 2 750 |
失去第四个电子 | 9 550 | 11600 |
①通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子所需的能量远远大于失去第一个电子所需的能量。
____________________________。
②表中X可能为以上13种元素中的__________ (填写字母)元素。用元素符号表示X和j形成化合物的化学式: __________。
③Y是周期表中__________族元素。
④以上13种元素中, __________ (填写字母)元素原子失去核外第一个电子需要的能量最多。